依据下列条件能将某溶液的物质的量浓度计算出来的是( )
①每10 mL溶液中含有0.23 g Na+的硫酸钠溶液
②每10个水分子中溶有1个Na+的NaOH溶液
③浓度为18.4 mol·L-1的硫酸10 mL加到100 mL水中所得的稀硫酸
④标准状况下,100 mL氨气溶于20 mL水中所得溶液的密度为0.9 g·cm-3的氨水
| A.①② | B.①③ | C.①④ | D.②③ |
设NA为阿伏加德罗常数的数值,下列说法不正确的是( )
| A.常温下,1 L pH=1的硫酸溶液中含有的H+为0.1NA |
| B.常温下,14 g C2H4和C3H6的混合气体中含有2NA个氢原子 |
| C.2.3 g Na和足量的O2完全反应,在常温和燃烧时,转移电子数均为0.1NA |
| D.1 mol甲醇中含有C—H键的数目为NA |
下列叙述的两个量,一定相等的是( )
| A.质量相等的金刚石和C60中的碳原子数目 |
| B.0.1 mol/L NaCl溶液与0.05 mol/L Na2CO3溶液中所含Na+的数目 |
| C.标准状况下等体积的SO2和SO3的分子数目 |
| D.等体积pH都为3的稀盐酸与FeCl3溶液中,由水电离产生的H+数目 |
室温时,甲、乙两同学在实验室配制氯化钠溶液。甲同学配制5%的NaCl溶液100 g,乙同学配制0.5 mol/L的NaCl溶液100 mL(20 ℃时,氯化钠的溶解度为36 g)。下列说法正确的是( )
| A.两同学所需溶质的质量相同 |
| B.两同学所需实验仪器种类相同 |
| C.两同学所配溶液均为不饱和溶液 |
| D.两同学所配溶液的质量相同 |
下列说法中正确的是( )。
| A.6.8 g熔融KHSO4与3.9 g熔融Na2O2中阴离子数目相同 |
B.某金属阳离子的结构示意图为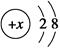 ,其与Cl-形成的强电解质都是离子化合物 ,其与Cl-形成的强电解质都是离子化合物 |
C.二硫化碳是直线形非极性分子,其电子式为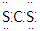 |
| D.中子数为18的氯原子可表示为18Cl |
下列说法一定正确的是
A.反应A(s)  2B(g) + C(g),当C的体积分数不变时,反应达到平衡状态 2B(g) + C(g),当C的体积分数不变时,反应达到平衡状态 |
| B.将钢闸门与直流电源的正极相连,可防止钢闸门腐蚀 |
| C.将33.6LNO2溶于D2O中得到1L溶液,该溶液的物质的量浓度为1.0mol/L |
| D.在一定条件下,催化分解80g SO3,混合气体中氧原子数为3×6.02×1023 |
设NA为阿伏加德罗常数。下列叙述不正确的是
| A.标准状况下,2.24 L Cl2完全溶于足量的水中,转移电子的数目为0.1NA |
| B.常温常压下,11.0g C3H8中含有共价键的数目为2.5NA |
| C.常温常压下,1 L 0.1 mol·L-1 NH4NO3溶液中NO3-的数目为0.1NA |
| D.30g甲醛(HCHO)和醋酸的混合物中含碳原子数目为NA |
用NA表示阿伏加德罗常数的值。下列叙述正确的是
| A.常温常压下,NO2和N2O4的混合物46g中含有2NA个氧原子 |
| B.常温常压下的33.6L氯气与27g铝充分反应,转移电子数为3NA |
| C.10mL98%的浓H2SO4用水稀释至l00mL,H2SO4的质量分数为9.8% |
| D.标准状况下,80g SO3中含3NA个氧原子,体积约为22.4L |
下列有关化学用语使用正确的是
A.次氯酸的结构式: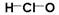 |
B.四氯化碳分子球棍模型:  |
C.甲基的电子式: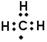 |
| D.油酸的分子式:C18H32O2 |