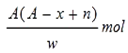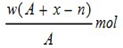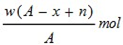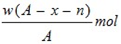用一充满氨气的烧瓶做喷泉实验,当水充满整个烧瓶后,烧瓶内氨水的物质的量浓度是(按标准状况下计算)( )
| A.0.045 mol·L-1 | B.1 mol·L-1 |
| C.0.029 mol·L-1 | D.不能确定 |
下列说法正确的是( )
| A.39K+和40Ca2+微粒中的电子数和中子数都相等 |
| B.在标准状况下,若D2和He体积相等,则质量不相等 |
| C.7.8 g Na2O2与足量的CO2反应时失去的电子数为0.2 NA |
| D.把1 mol NaCl溶于1 L水中,所得NaCl溶液的物质的量浓度为1mol/L |
下列表达方式错误的是( )
| A.H∶Cl | B. | C.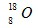 | D.O=C=O |
在标准状况下,用干燥烧瓶收集一瓶氯化氢气体倒置于盛水的水槽中时,水充满烧瓶(假设烧瓶里溶液不扩散出水槽),烧瓶里盐酸的密度为ρ g·cm-3。该盐酸的物质的量浓度、溶质的质量分数分别为( )。
A.c=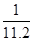 mol·L-1、w= mol·L-1、w=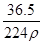 % % |
B.c=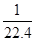 mol·L-1、w= mol·L-1、w=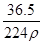 % % |
C.c=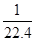 mol·L-1、w= mol·L-1、w=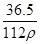 % % |
D.c=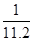 mol·L-1、w= mol·L-1、w=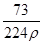 % % |
实验中需用2.0 mol·L-1的Na2CO3溶液950 mL,配制时应选用容量瓶的规格和称取Na2CO3固体的质量分别为 ( )。
| A.950 mL;201.4 g | B.1 000 mL;212.0 g |
| C.100 mL;21.2 g | D.500 mL;100.7 g |
设NA为阿伏加德罗常数的数值,下列各项叙述中正确的有( )。
①0.2 mol H2O2完全分解转移的电子数为0.4NA
②25 ℃、101 kPa下,16 g O3和O2混合气体中含有的氧原子数为NA
③将含0.1 mol FeCl3的饱和溶液滴入沸水形成的胶体粒子的数目为0.1NA
④1 mol N2和3 mol H2在一定条件下的密闭容器中充分反应,容器内的分子数大于2NA
| A.①②③ | B.①②④ | C.①②③④ | D.②④ |
用NA表示阿伏加德罗常数的值,下列叙述正确的是( )。
| A.等质量的N2和CO所含分子数均为NA |
| B.在标准状况下,22.4 L CH4与18 g H2O所含的电子数均为10NA |
| C.一定温度下,1 L 1 mol·L-1的CH3COONa溶液含NA个CH3COO- |
| D.1 mol SO2与足量O2在一定条件下反应生成SO3,共转移2NA个电子 |
用NA代表阿伏加德罗常数的数值,下列说法正确的是 ( )。
| A.标准状况下,22.4 L CHCl3中含有的氯原子的数目为3NA |
| B.7 g CnH2n中含有的氢原子数目为NA |
| C.18 g D2O中含有的质子数目为10NA |
| D.0.5 mol·L-1 Na2CO3溶液中含有的CO32-的数目为0.5NA |