0 95634 95642 95648 95652 95658 95660 95664 95670 95672 95678 95684 95688 95690 95694 95700 95702 95708 95712 95714 95718 95720 95724 95726 95728 95729 95730 95732 95733 95734 95736 95738 95742 95744 95748 95750 95754 95760 95762 95768 95772 95774 95778 95784 95790 95792 95798 95802 95804 95810 95814 95820 95828 203614

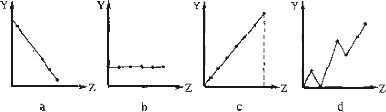


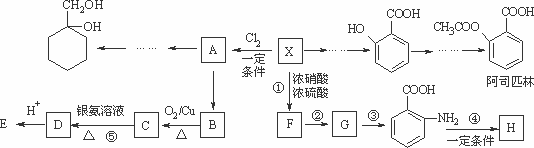
 (水杨酸)有多种同分异构体,写出符合下列条件的结构简式________.
(水杨酸)有多种同分异构体,写出符合下列条件的结构简式________. 最合理的方案(不超过4步).例:
最合理的方案(不超过4步).例: