0 95621 95629 95635 95639 95645 95647 95651 95657 95659 95665 95671 95675 95677 95681 95687 95689 95695 95699 95701 95705 95707 95711 95713 95715 95716 95717 95719 95720 95721 95723 95725 95729 95731 95735 95737 95741 95747 95749 95755 95759 95761 95765 95771 95777 95779 95785 95789 95791 95797 95801 95807 95815 203614

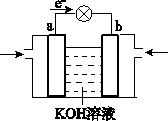
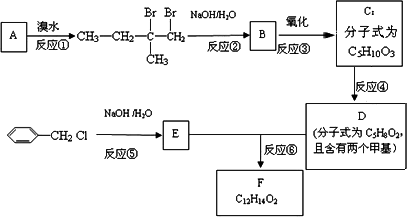
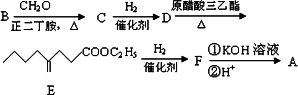

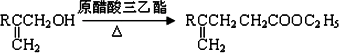

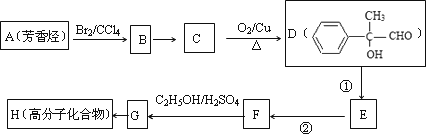
 的合成线路如图所示:
的合成线路如图所示: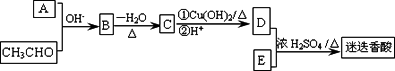
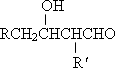
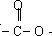 的基团.符合上述条件的D的同分异构体有:
的基团.符合上述条件的D的同分异构体有: