|
常温下,0.1 mol/L氨水溶液中 | |
A. |
该溶液中氢离子的浓度:c(H+)=1×10-9 mol/L |
B. |
0.1 mol/L氨水溶液与0.1 mol/L HCl溶液等体积混合后所得溶液中: c(NH4+)+c(H+)=c(Cl-)+c(OH-) |
C. |
0.1 mol/L的氨水溶液与0.05 mol/L H2SO4溶液等体积混合后所得溶液中:c(NH4+)+c(NH3)+c(NH3·H2O)=2c(SO42-) |
D. |
浓度均为0.1 mol/L的NH3·H2O和NH4Cl溶液等体积混合后,若溶液呈碱性,则c(NH4+)>c(NH3·H2O)>c(Cl-)>c(OH-)>c(H+) |
|
已知NO2遇水发生反应:2NO2+H2O→HNO2+HNO3.实验证明将NO2通入水中会逸出NO气体,而通入NaOH溶液中则可完全被吸收,通入Na2CO3溶液中只逸出CO2.下列说法错误的是 | |
A. |
HNO2非常不稳定,其分解产物为NO和H2O |
B. |
NO2与水的反应机理:NO2先与水发生岐化反应生成HNO2和HNO3,HNO2再分解 |
C. |
HNO2的酸性弱于碳酸的酸性 |
D. |
NO2通入NaOH溶液中,生成的HNO2和HNO3都与NaOH发生中和反应 |
|
在8.08 g铁与铜的混和物中,加入200 mL 0.6 mol/L的稀硝酸,充分反应后剩余金属5.44 g.再向其中加入50 mL 0.4 mol/L的稀硫酸,充分振荡后剩余金属4.48 g.若硝酸的还原产物只有NO,下列说法正确的是 | |
A. |
剩余的5.44 g金属为铁 |
B. |
剩余5.44 g金属为铜 |
C. |
共生成NO气体0.03 mol |
D. |
8.08 g金属中铁的质量分数为0.208 |
|
向NaOH(aq)滴入HAc(aq)的过程中,溶液中离子浓度的大小可能正确的是 | |
A. |
c(OH-)=c(Na+)>c(Ac-)>c(H+) |
B. |
c(Na+)>c(OH-)=c(Ac-)>c(H+) |
C. |
c(Na+)>c(Ac-)>c(OH-)>c(H+) |
D. |
c(H+)>c(Ac-)>c(Na+)>c(OH-) |
|
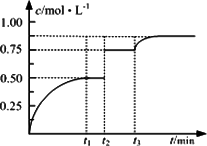
一定温度下,将1 mol A(g)和1 mol B(g)充入2 L密闭容器中发生反应,在t1时达到平衡:A(g)+B(g)
| |
A. |
反应方程式中x=2 |
B. |
t2时刻改变的条件是使用催化剂 |
C. |
t3时刻改变的条件是移去少量D |
D. |
t1~t3间该反应的平衡常数相同 |
|
Na2SO3溶液做为吸收液吸收SO2时,吸收液pH随n(SO32-)∶n(HSO3-)变化的关系如下表:
以下离子浓度关系的判断正确的是 | |
A. |
NaHSO3溶液中c(H+)>c(OH-) |
B. |
Na2SO3溶液中c(Na+)>c(SO32-)>c(HSO3-)>c(OH-)>c(H+) |
C. |
当吸收液呈中性时,c(Na+)>c(SO32-)>c(HSO3-)>c(OH-)=c(H+) |
D. |
当吸收液呈中性时,c(Na+)=c(HSO3-)+2c(SO32-) |
|
甲、乙、丙、丁四种易溶于水的物质,分别由Na+、Ba2+、Al3+、H+、OH-、Cl-、HCO3-、SO42-中的不同阳离子和阴离子各一种组成,已知:①0.1 mol/L甲溶液中c(H+)>0.1 mol/L;②将少量乙溶液分别滴入其他三种物质的溶液时,均有白色沉淀生成;③向丙溶液中滴入AgNO3溶液有不溶于稀HNO3的白色沉淀生成,下列判断正确的是 | |
A. |
甲溶液含有SO42- |
B. |
乙溶液含有SO42- |
C. |
丙溶液显酸性 |
D. |
丁溶液显酸性 |
|
将足量CO2通入下列各溶液中,所含离子还能大量共存的是 | |
A. |
Na+、SO42-、C6H5O-、Cl- |
B. |
Na+、CO32-、NO3-、Br- |
C. |
Al3+、Cl-、SO42-、I- |
D. |
K+、AlO2-、NO3-、SO42- |
|
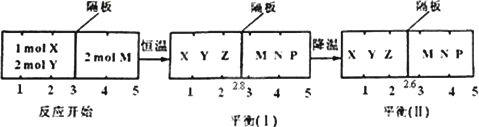
可逆反应①X(g)+2Y(g)
下列判断正确的是 | |
A. |
反应①的正反应是吸热反应 |
B. |
达平衡(Ⅰ)时体系的压强与反应开始时体系的压强之比为14∶15 |
C. |
在平衡(Ⅰ)和平衡(Ⅱ)中M的体积分数相等 |
D. |
达平衡(Ⅰ)时,X的转化率为 |