|
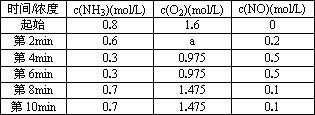
在1 L密闭容器中发生反应:4NH3(g)+5O2(g)
下列说法错误的是 | |
A. |
反应在第2 min到第4 min时,O2的平均反应速率为0.1875 mol/(L·min) |
B. |
反应在第2 min时改变了某一条件,该条件可能是使用催化剂或升高温度 |
C. |
第4 min时、第8 min时分别达到化学平衡,且平衡常数不相同 |
D. |
在开始反应的前2 min内,该反应的△H=-0.05Q kJ·mol-1 |
|
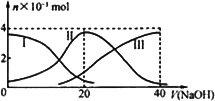
常温下,向20 mL 0.2 mol/L H2A溶液中滴加0.2 mol/L NaOH溶液.有关微粒的物质的量变化如下图(其中Ⅰ代表H2A,Ⅱ代表HA-,Ⅲ代表A2-).根据图示判断,下列说法正确的是
| |
A. |
当V(NaOH)=20 mL时,溶液中离子浓度大小关系:c(Na+)>c(HA-)>c(H+)>c(A2-)>c(OH-) |
B. |
等体积等浓度的NaOH溶液与H2A溶液混合后,其溶液中水的电离程度比纯水的大 |
C. |
NaHA溶液中:c(OH-)+c(A2-)=c(H+)+c(H2A) |
D. |
向Na2A溶液加入水的过程中,pH可能增大也可能减小 |
|
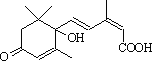
用S-诱抗素制剂,可以保证鲜花盛开.S-诱抗素的结构如图,下列关于该物质的说法正确的是
| |
A. |
其分子中含有一个手性碳原子 |
B. |
既能发生加聚反应,又能发生缩聚反应 |
C. |
1 mol该物质与NaOH溶液反应,最多消耗2 mol NaOH |
D. |
既可以与FeCl3溶液发生显色反应,又可以使酸性KMnO4溶液褪色 |
|
某无色溶液可能存在Al3+、H+、Na+、SO | |
A. |
一定存在的离子是Na+、SO |
B. |
可能存在的离子是Al3+、CO |
C. |
一定存在的离子是Na+、SO |
D. |
可能存在的离子是CO |
|
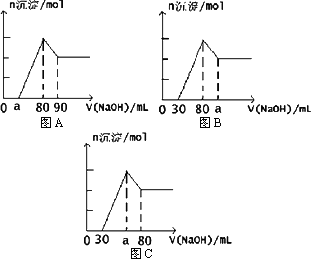
把一块镁铝合金投入到1 mol/L HCl溶液里,待合金完全溶解后,往溶液里加入1 mol/LNaOH溶液,生成沉淀的物质的量随加入NaOH溶液体积变化的关系如图A所示.下列说法不正确的是
| |
A. |
A图中a的取值范围为0≤a<50 |
B. |
A图中n(Mg)/n(Al)的最大值为2.5 |
C. |
若将关系图改为B图时,则a的取值范围为80<a<90 |
D. |
若将关系图改为C图时,则a的取值范围为67.5<a<80 |
|
工业上以铬铁矿(主要成分为FeO·Cr2O3)、碳酸钠、氧气和硫酸为原料生产重铬酸钠(Na2Cr2O7·2H2O),其主要反应为: (1)4FeO·Cr2O3+8Na2CO3+7O2 (2)2Na2CrO4+H2SO4 下列说法中正确的是 | |
A. |
反应(1)和(2)均为氧化还原反应 |
B. |
反应(1)的氧化剂是O2,还原剂是FeO·Cr2O3 |
C. |
高温下,O2的氧化性大于Fe2O3小于Na2CrO4 |
D. |
生成1 mol的Na2Cr2O7时共转移7 mol电子 |
|
a g Mg、Al合金完全溶解在C1 mol·L-1、V1L HCl溶液中,产生b g H2.再向反应后的溶液中加入C2 mol·L-1、V2 L NaOH溶液,恰好使沉淀达到最大值,且沉淀质量为d g.下列关系错误的是 | |
A. |
d=a+17b |
B. |
C1=C2V2/V1 |
C. |
铝为(24b-a)/9 mol |
D. |
与金属反应后剩余盐酸为(C1V1-2b)mol |
|
甲、乙、丙、丁四种易溶于水的物质,分别由NH ①将甲溶液分别与其他三种物质的溶液混合,均有白色沉淀生成; ②0.1 mol/L乙溶液中c(H+)>0.1 mol/L; ③向丙容器中滴入AgNO3溶液又不溶于稀HNO3的白色沉淀生成, 下列结论不正确的是 | |
A. |
甲溶液含有Ba2+ |
B. |
乙溶液含有SO |
C. |
丙溶液含有Cl- |
D. |
丁溶液含有Mg2+ |
|
下列离子方程式中正确的是 | |
A. |
向NaHSO4溶液中逐滴加入Ba(OH)2溶液,至SO42-沉淀完全; 2H++SO42-+Ba2++2OH- |
B. |
碳酸钠与醋酸溶液反应:CO32-+2H+ |
C. |
氢氧化亚铁与硝酸溶液混合:Fe(OH)2+2H+ |
D. |
在Ba(OH)2溶液中滴加少量NaHCO3溶液:HCO3-+Ba2++OH- |
|
在溶液中可以大量共存,加OH-产生沉淀,加H+生成气体的一组离子是 | |
A. |
Na+、Cu2+、CO32-、Cl- |
B. |
Na+、Cl-、HCO3-、Mg2+ |
C. |
Cl-、NO3-、K+、Ca2+ |
D. |
NH4+、K+、H+、SO42- |