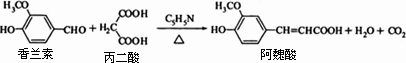|
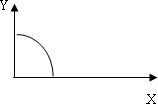
在一定条件下,固定容积的密闭容器中反应:2NO2(g)
| |
A. |
当X表示温度时,Y表示NO2的物质的量 |
B. |
当X表示压强时,Y表示NO2的转化率 |
C. |
当X表示反应时间时,Y表示混合气体的密度 |
D. |
当X表示NO2的物质的量时,Y表示O2的物质的量 |
|
下列离子方程式中正确的是 | |
A. |
NaHSO4与Ba(OH)2溶液反应至中性: Ba2++2OH-+2H++SO42-→BaSO4↓+2H2O |
B. |
NH4HCO3溶液与过量NaOH溶液反应:NH4++OH-→NH3·H2O |
C. |
HAc溶液与KOH溶液反应:HAc+OH-→Ac-+H2O |
D. |
含有0.1 mol FeI2的溶液中通入标准状况下2.24 L Cl2 2Fe2++2I-+2Cl2→2Fe3++I2+4Cl- |
|
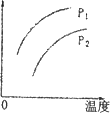
在容积一定的密闭器中发生可逆反应A(g)+2B(g)
| |
A. |
P1<P2,纵坐标指A的质量分数 |
B. |
P1>P2,纵坐标指C的质量分数 |
C. |
P1<P2,纵坐标指混合气体的平均摩尔质量 |
D. |
P1>P2,纵坐标指A的转化率 |
|
下列叙述正确的是 | |
A. |
c(NH |
B. |
无色透明的酸性溶液中,Cu2+、K+、SO |
C. |
0.2 mol·L-1 HCl溶液与等体积0.05 mol·L-1 Ba(OH)2溶液混合后,溶液的pH=1 |
D. |
NaHCO3溶液中:c(H+)+c(H2CO3)=c(CO |
|
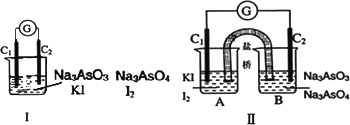
下图Ⅰ、Ⅱ分别是甲、乙两组同学将反应“AsO
下列叙述中正确的是 | |
A. |
甲组操作时,微安表(G)指针发生偏转 |
B. |
甲组操作时,溶液颜色变深 |
C. |
乙组操作时,C2做正极 |
D. |
乙组操作时,C1上发生的电极反应为I2+2e-=2I- |
|
在温度、容积相同的3个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下(已知N2(g)+3H2(g)=2NH3(g) ΔH=-92.4 KJ·mol-1)
下列说法正确的是 | |
A. |
2c1>c3 |
B. |
a+b=92.4 |
C. |
2p2<p3 |
D. |
α1+α3<1 |
|
已知A、B、C、D、E是短周期中原子序数依次增大的5种主族元素,其中元素A、E的单质在常温下呈气态,元素B的原子最外层电子数是其电子层数的2倍,元素C在同周期的主族元素中原子半径最大,元素D的合金是日常生活中常用的金属材料.下列说法正确的是 | |
A. |
元素A、B组成的化合物常温下一定呈气态 |
B. |
一定条件下,元素C、D的最高价氧化物对应的水化物之间能发生反应 |
C. |
工业上常用电解法制备元素C、D、E的单质 |
D. |
化合物AE与CE古有相同类型的化学键 |
|
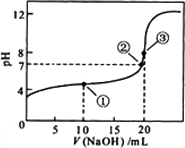
常温下,用0.1000 mol·L -1 NaOH溶液滴定20.00 mL 0.1000 mol·L-1 CH3COOH溶液所得滴定曲线如下图.下列说法正确的是
| |
A. |
点①所示溶液中:c(CH3COO-)+(OH-)=c(CH3COOH)+c(H+) |
B. |
点②所示溶液中:c(Na+)=c(CH3COOH)+c(CH3COO-) |
C. |
点③所示溶液中:c(Na+)>c(OH-)>c(CH3COO-)>c(H+) |
D. |
滴定过程中可能出现:c(CH3COOH)>c(CH3COO-)>c(H+)>c(Na+)>(OH-) |
|
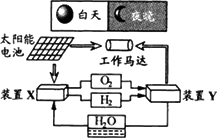
下图是一种航天器能量储存系统原理示意图.
下列说法正确的是 | |
A. |
该系统中只存在3种形式的能量转化 |
B. |
装置Y中负极的电极反应式为:O2+2H2P+4e-=4OH- |
C. |
装置X能实现燃料电池的燃料和氧化剂再生 |
D. |
装置X、Y形成的子系统能实现物质的零排放,并能实现化学能与电能间的完全转化 |
|
阿魏酸在食品、医药等方面有着广泛用途.一种合成阿魏酸的反应可表示为
下列说法正确的是 | |
A. |
可用酸性KMnO4溶液检测上述反应是否有阿魏酸生成 |
B. |
香兰素、阿魏酸均可与Na2CO3 、NaOH溶液反应 |
C. |
通常条件下,香兰素、阿魏酸都能发生取代、加成、消去反应 |
D. |
与香兰素互为同分异构体,分子中有4种不同化学环境的氢,且能发生银镜反应的酚类化合物共有2种 |