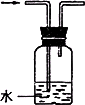|
设NA表示阿伏加德罗常数,下列叙述中正确的是 | |
A. |
80 g硝酸铵含有氮原子数为2NA |
B. |
常温常压下,22.4 L的D2、H2组成的气体分子数为NA |
C. |
标准状况下,22.4 L SO3中含有的氧原子数为0.3NA |
D. |
1 mol Na2O2与足量CO2反应转移的电子数NA |
|
在石灰窑中烧制生石灰,1 mol CaCO3完全分解所需要的能量,可燃烧0.453 mol碳来提供.设空气中O2体积分数为0.21,N2为0.79,则石灰窑产生的气体中CO2的体积分数可能是 | |
A. |
0.43 |
B. |
0.46 |
C. |
0.49 |
D. |
0.52 |
|
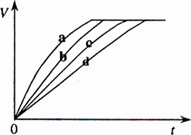
等质量的铁与过量的盐酸在不同的试验条件下进行反应,测定在不同时间t产生氢气体积v的数据,根据数据绘制得到下图,则曲线a、b、c、d所对应的试验组别可能是
| |
A. |
4-3-2-1 |
B. |
1-2-3-4 |
C. |
3-4-2-1 |
D. |
1-2-4-3 |
|
下列离子方程式书写正确的是 | |
A. |
AgNO3溶液中滴入少量的Na2S溶液2Ag++S2-→Ag2S↓ |
B. |
过量CO2通入Ca(ClO)2溶液中ClO-+CO2+H2O→HCO3-+HClO |
C. |
向Na2CO3溶液中加入过量CH3COOH溶液CO32-+2H+→CO2↑+H2O |
D. |
向Ba(OH)2溶液中加入少量NaHSO3溶液2HSO3-+Ba2++2OH-→BaSO3↓+SO32-+2H2O |
|
研究发现,空气其中少量的NO2能参与硫酸型酸雨的形成,反应过程如下: ①SO2+NO2→SO3+NO ②SO3+H2O→H2SO4 ③2NO+O2→2NO2 NO2在上述过程中的作用,与H2SO4在下列变化中的作用相似的是 | |
A. |
潮湿的氯气通过盛有浓H2SO4的洗气瓶 |
B. |
硫化氢通入浓H2SO4中 |
C. |
浓H2SO4滴入萤石中,加热 |
D. |
加入少量H2SO4使乙酸乙酯水解 |
|
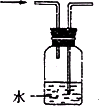
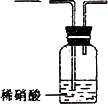
设计学生试验要注意安全、无污染、现象明显.根据启普发生器原理,可用底部有小孔的试管制简易的气体发生器(见下图).若关闭K,不能使反应停止,可将试管从烧杯中取出(会有部分气体逸出).下列气体的制取宜使用该装置的是
| |
A. |
用二氧化锰(粉末)与双氧水制氧气 |
B. |
用锌粒与稀硫酸制氢气 |
C. |
用硫化亚铁(块状)与盐酸制硫化氢 |
D. |
用碳酸钙(块状)与稀硫酸制二氧化碳 |
|
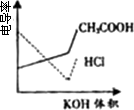
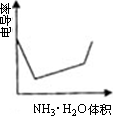
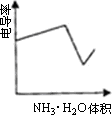
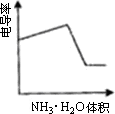
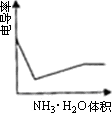
电导率是衡量电解质溶液导电能力大小的物理量,根据溶液电导率变化可以确定滴定反应的终应.下图是KOH溶液分别滴定HCl溶液和CH3COOH溶液的滴定曲线示意图.下列示意图中,能正确表示用NH3·H2O溶液滴定HCl和CH3COOH混合溶液的滴定曲线的是
| |
A. |
|
B. |
|
C. |
|
D. |
|
|
盐酸、醋酸和碳酸氢钠是生活中常见的物质.下列表述正确的是 | |
A. |
在NaHCO3溶液中加入与其等物质的量的NaOH,溶液中的阴离子只有CO |
B. |
NaHCO3溶液中:e(H+)+e(H2CO3)=c(OH-) |
C. |
10 mL 0.10 mol·L-1 CH3COOH溶液加入等物质的量的NaOH后,溶液中离子的浓度由大到小的顺序是:c(Na+)>c(CH3COO-)>c(OH-)>c(H+) |
D. |
中和体积与pH都相同的HCl溶液和CH3COOH溶液所消耗的NaOH物质的量相同 |