|
下列用来表示物质变化的反应式中,错误的是 | |
A. |
NH4HCO3溶液与过量KOH溶液反应的离子方程式: NH4++HCO3-+2OH-=NH3·H2O+CO32-+H2O |
B. |
向KHSO4溶液中滴入Ba(OH)2溶液使pH=7的离子方程式: SO42-+H++Ba2++OH-=BaSO4↓+H2O |
C. |
明矾水解的离子方程式:Al3++3H2O |
D. |
K37ClO3与浓盐酸(HCl)在加热时生成氯气的化学方程式: K37ClO3+6HCl=K37Cl+3Cl2↑+3H2O |
|
下列各组离子在相应的条件下可以大量共存的是 | |
A. |
在碱性溶液中:CO32-、K+、C1-、Ca2+ |
B. |
与铝粉反应放出氢气的无色溶液中:NO3-、Mg2+、Na+、SO42- |
C. |
在c(H+)/c(OH-) |
D. |
在中性溶液中:Fe3+、S2-、NO3-、A13+ |
|
某溶液中含HCO3-、SO32-、CO32-、NO3-、Na+等五种离子,若向其中加入足量Na2O2后(设溶液体积不变),溶液中上述离子浓度基本保持不变的是 | |
A. |
NO3- |
B. |
SO32-、NO3- |
C. |
CO32-、NO3- |
D. |
CO32-、NO3-、Na+ |
|
下列各组离子能大量共存,当溶液中C(H+)=10-1 mol·L-1时,有气体产生;而当溶液中C(H+)=10-13 mol·L-1时,又能生成沉淀.则该组离子可能是: | |
A. |
Na+、Cu2+、NO3-、CO32- |
B. |
Ba2+、K+、Cl-、HCO3- |
C. |
Fe2+、Na+、SO42-、NO3- |
D. |
Mg2+、NH4+、SO42-、Cl- |
|
有关3BrF3+5H2O=HBrO3+Br2+9HF+O2反应的叙述,正确的是 | |
A. |
还原剂与氧化剂的物质的量之比为5∶3 |
B. |
HBrO3和HF是还原产物 |
C. |
生成1 mol O2,转移了6 mol电子 |
D. |
BrF3既是氧化剂又是还原剂 |
|
设NA为阿伏加德罗常数.下列叙述中正确的是 | |
A. |
标准状况下,22.4 L CO2和O2混合气体中含有的氧原子数约为NA |
B. |
常温常压下,0.1 mol铁在0.1 mol Cl2中充分燃烧,转移的电子数为0.3NA |
C. |
2 mol SO2和1 mol O2混合在V2O5存在的条件下密闭容器中加热反应后,容器内物质分子数大于2NA |
D. |
1 L 1 mol/L的K2CO3溶液中离子总数大于3NA |
|
下列有关溶液中所含物质或离子的检验,判断正确的是 | |
A. |
加入AgNO3溶液生成的白色沉淀不溶于稀盐酸,则原溶液中一定有Cl-存在 |
B. |
加入数滴新制的Cu(OH)2浊液并加热,出现红色沉淀,则原溶液中一定有葡萄糖 |
C. |
加入盐酸有能使澄清石灰水变浑浊的气体产生,则原溶液中一定有CO32-存在 |
D. |
加入氨水时生成白色沉淀,当氨水过量时白色沉淀消失,则原溶液中一定无Al3+存在 |
|
对下列定量实验中的基本操作和仪器的描述正确的是 | |
A. |
用托盘天平称取0.5 mol NaOH固体20.0 g; |
B. |
将用水润湿的pH试纸,浸入稀盐酸溶液,测定溶液的pH值; |
C. |
用瓷坩锅灼烧各种钠的化合物 |
D. |
在配制一定物质的量浓度的溶液时,定容后,经摇匀发现液面低于刻度线,此时无须再加入蒸馏水使其液面与刻度持平 |
|
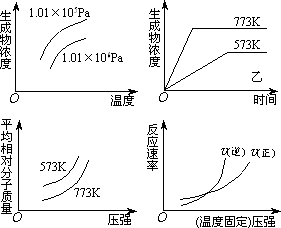
现有下列四个图像:
下列反应中全部符合上述图像的反应是 | |
A. |
N2(g)+3H2(g) |
B. |
2SO3(g) |
C. |
4NH3(g)+5O2(g) |
D. |
H2(g)+CO(g) |
|
以Fe为阳极,石墨棒为阴极,对足量的Na2SO4溶液进行电解,一段时间后得到1 mol Fe(OH)3沉淀,此间共消耗水的物质的量为: | |
A. |
1.5 mol |
B. |
2 mol |
C. |
2.5 mol |
D. |
3 mol |