|
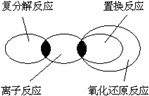
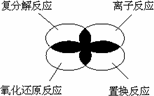
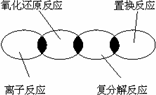
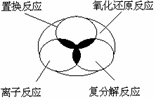
在海水中提取溴的反应原理是5NaBr+NaBrO+3H2SO4=3Br2+3Na2SO4+3H2O下列反应的原理与上述反应最相似的是: | |
A. |
2NaBr+Cl2=2NaCl+Br2 |
B. |
2FeCl3+H2S=2FeCl2+S+2HCl |
C. |
2H2S+SO2=3S+2H2O |
D. |
AlCl3+3NaAlO3+6H2O=4Al(OH)3+3NaCl |
|
ClO2是一种消毒杀菌效率高、二次污染小的水处理剂.实验室可通过以下反应制得ClO2:2KClO3+H2C2O4+H2SO4 | |
A. |
KClO3在反应中得到电子 |
B. |
ClO2是氧化产物 |
C. |
H2C2O4在反应中被氧化 |
D. |
1 mol KClO3参加反应有2 mol电子转移 |
|
已知I-、Fe2+、SO2、Cl-和H2O2均有还原性,它们在酸性溶液中还原性的强弱顺序为Cl-<Fe2+<H2O2<I-<SO2,则下列反应不能发生的是 | |
A. |
2Fe3++SO2+2H2O=2Fe2++SO42-+4H+ |
B. |
I2+SO2+2H2O=H2SO4+2HI |
C. |
H2O2+H2SO4=SO2+O2+2H2O |
D. |
2Fe2++I2=2Fe3++2I- |
|
有BaCl2和NaCl的混合溶液a L,将它均分成两份.一份滴加稀硫酸,使Ba2+离子完全沉淀;另一份滴加AgNO3溶液,使Cl-离子完全沉淀.反应中消耗x mol H2SO4、y mol AgNO3.据此得知原混合溶液中的c(Na+)/mol·L-1为 | |
A. |
(y-2x)/a |
B. |
(y-x)/a |
C. |
(2y-2x)/a |
D. |
(2y-4x)/a |
|
下列有关溶液性质的叙述,正确的是 | |
A. |
室温时饱和的二氧化碳水溶液,冷却到0℃时会放出一些二氧化碳气体 |
B. |
强电解质在水中溶解度一定大于弱电解质 |
C. |
相同温度下,把水面上的空气换成相同压力的纯氧,100 g水中溶入氧气的质量增加 |
D. |
将40℃的饱和硫酸铜溶液升温至50℃,或者温度仍保持在40℃并加入少量无水硫酸铜,在这两种情况下溶液中溶质的质量分数均保持不变. |
|
下列各组离子能大量共存,当溶液中C(H+)=10-1 mol·L-1时,有气体产生;而当溶液中C(H+)=10-13 mol·L-1时,又能生成沉淀.则该组离子可能是: | |
A. |
Na+、Cu2+、NO3-、CO32- |
B. |
Ba2+、K+、Cl-、HCO3- |
C. |
Fe2+、Na+、SO42-、NO3- |
D. |
Mg2+、NH4+、SO42-、Cl- |
|
为除去混在氯化钾中的少量硫酸钾和氯化钙杂质,需进行下列六项操作: ①加水溶解 ②加热蒸发结晶 ③加入过量氯化钡溶液 ④加入过量盐酸 ⑤加入过量碳酸钾溶液 ⑥过滤,下列操作顺序正确的是 | |
A. |
①③⑤⑥④② |
B. |
①⑤③④⑥② |
C. |
①③④⑥⑤② |
D. |
①⑤③⑥④② |
|
R2O8n-离子在一定条件下可以把Mn2+离子氧化为MnO4-,若反应后R2O8n-离子变为RO42-离子,又知反应中氧化剂与还原剂的物质的量之比为5:2,则n的值是: | |
A. |
1 |
B. |
2 |
C. |
3 |
D. |
4 |
|
已知I-、Fe2+、SO2、Cl-和H2O2均有还原性,它们在酸性溶液中还原性的强弱顺序为Cl-<Fe2+<H2O2<I-<SO2,则下列反应不能发生的是 | |
A. |
2Fe3++SO2+2H2O=2Fe2++SO42-+4H+ |
B. |
I2+SO2+2H2O=H2SO4+2HI |
C. |
H2O2+H2SO4=SO2+O2+2H2O |
D. |
2Fe2++I2=2Fe3++2I- |