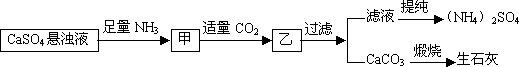|
科学家在高压下成功地将CO2转化为具有类似SiO2结构的晶体,下列关于CO2的原子晶体的说法正确的是 | |
A. |
CO2的分子晶体转化为原子晶体是化学变化 |
B. |
CO2的原子晶体和分子晶体实际上是同种物质 |
C. |
CO2的原子晶体和分子晶体具有相同的物理性质 |
D. |
在CO2的原子晶体中,每一个C原子周围结合4个O原子 |
|
最近,中国科大的科学家们将C60分子组装在一单层分子膜表面,在-268℃时冻结分子的热振荡,并利用扫描隧道显微镜首次“拍摄”到能清楚分辨碳原子间单、双键的分子图像.下列化合物分子中一定既含单键又含双键的是 | |
A. |
CO2 |
B. |
C2H4O |
C. |
COCl2 |
D. |
H2O2 |
|
盖斯定律认为:不管化学过程是一步完成或分数步完成,整个过程的总热效应相同.已知:H2O(g)=H2O(l) △H1=-Q1 kJ/mol C2H5OH(g)=C2H5OH(l) △H2=-Q2 kJ/mol C2H5OH(g)+3O2(g)=2CO2(g)+3H2O(g) △H3=-Q3 kJ/mol 若使23 g酒精液体完全燃烧,最后恢复到室温,则放出的热量为(单位均为kJ) | |
A. |
Q1+Q2+Q3 |
B. |
0.5(Q1+Q2+Q3) |
C. |
1.5Q1-1.5Q2+0.5Q3 |
D. |
1.5Q1-0.5Q2+0.5Q3 |
|
下列离子方程式正确的是 | |
A. |
硫酸铝溶液中加过量氨水:Al3++4OH-=AlO2-+2H2O |
B. |
向硅酸钠溶液中通入过量的CO2: |
C. |
过量铁粉与一定量稀硝酸反应:Fe+4H++NO3-=Fe3++NO↑+2H2O |
D. |
向NH4HSO4稀溶液中逐滴加入Ba(OH)2稀溶液至刚好沉淀完全: Ba2++2OH-+NH4++H++SO42-=BaSO4↓+NH3·H2O+H2O |
|
为了除去NO、NO2、N2O4对大气的污染,常采用氢氧化钠溶液进行吸收处理(反应方程式:3NO2+2NaOH→NaNO3+NaNO2+H2O;NO2+NO+2NaOH→2NaNO2+H2O).现有由a mol NO、b mol NO2、c mol N2O4组成的混合气体恰好被VL氢氧化钠溶液吸收(无气体剩余),则此氢氧化钠溶液的物质的量浓度最小为 | |
A. |
|
B. |
|
C. |
|
D. |
|
|
某混合气体可能有CO、CO2、NH3、HCl、H2和水蒸气中的一种或几种,当依次通过澄清石灰水(无浑浊现象)、氢氧化钡溶液(有浑浊现象)、浓硫酸、灼热的氧化铜(变红)和无水硫酸铜(变蓝)时,则可断定该混合气体中一定有 | |
A. |
CO2、HCl、H2 |
B. |
CO、H2、H2O |
C. |
CO、NH3、H2 |
D. |
CO、HCl、H2O |
|
某工厂用CaSO4、NH3、H2O、CO2制备(NH4)2SO4,其工艺流程如下:
下列推断不合理的是 | |
A. |
直接蒸干滤液得到纯净的(NH4)2SO4 |
B. |
生成1 mol (NH4)2SO4至少消耗2 mol NH3 |
C. |
CO2可被循环使用 |
D. |
往甲中通CO2有利于(NH4)2SO4生成 |
|
某无色溶液与NH4HCO3作用能产生气体,此溶液中可能大量共存的离子组是: | |
A. |
Cl-、H+、Cu2+、SO |
B. |
Na+、Ba2+、OH |
C. |
K+、NO |
D. |
NO |