|
对于平衡体系mA(g)+nB(g) | |
A. |
若温度不变,将容器的体积缩小到原来的一半,此时A的浓度为原来的2.1倍,则m+n>p+q |
B. |
若平衡时,A、B的转化率相等,说明反应开始时,A、B的物质的量之比为m∶n |
C. |
若m+n=p+q,则往含有a mol气体的平衡体系中再加入a mol的B,达到新平衡时,气体的总物质的量等于2a |
D. |
若温度不变时,压强增大到原来的2倍,达到新平衡时,总体积一定比原来的1/2要小 |
|
常温下,pH=9的CH3COONa溶液由水电离出来的C(H+)为a,pH=9的NH3·H2O溶液由水电离出来的C(H+)为b,下列a和b的关系正确的是 | |
A. |
a=b |
B. |
a=104b |
C. |
b=10-4a |
D. |
a=10-4b |
|
在铜的催化作用下氨气与氟气反应,得到一种三角锥形分子M和一种铵盐N.下列有关说法不正确的是 | |
A. |
该反应的化学方程式为4NH3+3F2=NF3+NH4F |
B. |
M是极性分子,其还原性比NH3强 |
C. |
M既是氧化产物,又是还原产物 |
D. |
N中既含有离子键,又含有共价键 |
|
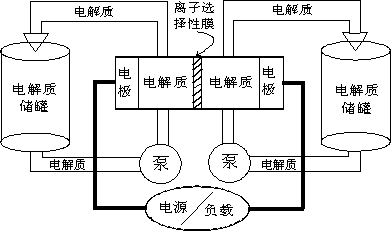
下图是一种正在投入生产的大型蓄电系统.左右两侧为电解质储罐,中央为电池,电解质通过泵不断在储罐和电池间循环;电池中的左右两侧为电极,中间为离子选择性膜,在电池放电和充电时该膜可允许钠离子通过;放电前,被膜隔开的电解质为Na2S2(右罐)和NaBr3(左罐),放电后,分别变为Na2S4和NaBr.下列说法正确的是
| |
A. |
电池充电时阳极电极反应式为:3Br--2e-=Br3- |
B. |
电池放电时,负极电极反应式为:2S22-+2e-=S42- |
C. |
电池放电时,电池的总反应方程式为:Na2S4+3NaBr=2Na2S2+NaBr3 |
D. |
在充电过程中Na+通过膜的流向为从左到右 |
|
某溶液中加入过量盐酸产生沉淀,滤液中再通入硫化氢又产生沉淀,不符合此现象的组是: | |
A. |
Hg2+、Al3+、Ba2+、Na+ |
B. |
Ag+、Fe3+、Mg2+、Cs+ |
C. |
Ag+、Cu2+、Rb+、NH4+ |
D. |
Fe2+、Ca2+、Li+、K+ |
|
历史上最早使用的还原性染料是靛蓝,其结构式如图,下列关于它的性质的叙述中错误的是
| |
A. |
它的苯环上的一氯取代物有4种 |
B. |
它的分子式是C16H10N2O2 |
C. |
它是高分子化合物 |
D. |
它可使溴水褪色 |
|
粗盐中含有可溶性杂质CaCl2、MgCl2和Na2SO4,若要得到纯净的NaCl固体,有如下实验操作:①加入过量Ba(OH)2溶液、②加入过量NaOH溶液、③加入过量BaCl2溶液、④加入过量Na2CO3溶液、⑤加入过量盐酸、⑥过滤、⑦蒸发结晶.正确的实验操作顺序是 | |
A. |
③②④⑥⑤⑦ |
B. |
③④②⑤⑦ |
C. |
②③④⑤⑥⑦ |
D. |
①④⑥⑤⑦ |
|
已知NaHSO3溶液和Na2CO3溶液混合后加热煮沸能产生CO2气体.现有浓度均为0.1 mol/L的NaHSO3溶液和NaHCO3溶液,两溶液中各粒子物质的量浓度的关系一定正确的是(R表示S或C) | |
A. |
c(Na+)+c(H+)=c(HRO3-)+c(RO32-)+c(OH-) |
B. |
c(H+)+c(H2RO3)=c(RO32-)+c(OH-) |
C. |
c(Na+)>c(HRO3-)>c(H+)>c(OH-)>c(RO32-) |
D. |
c(HRO3-)>c(H2RO3)>c(OH-)>c(RO32-)>c(H+) |