|
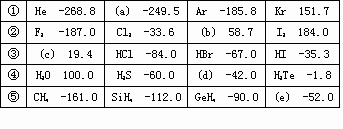
有五个系列同族元素的物质,101.3kP时测定它们的沸点(℃)如下表所示:
对应表中内容,下列叙述中正确的是 | |
A. |
a、b、c的化学式分别为Ne、Br2、HF |
B. |
系列②物质均有氧化性;系列③物质对应水溶液均是强酸 |
C. |
系列④中各化合物的稳定性顺序为:H20>H2S>H2Se>H2Te |
D. |
上表内物质HF和H2O,由于氢键的影响,其分子特别稳定 |
|
pH值相等的盐酸(甲)和醋酸(乙),分别与锌反应,若最后锌已全部溶解且放出气体一样多,为此下列说法正确的是 | |
A. |
反应开始时的速率:甲=乙 |
B. |
反应所需时间:甲<乙 |
C. |
反应开始时,酸的物质的量浓度:甲<乙 |
D. |
反应结速时,pH值:甲<乙 |
|
已知在1×105Pa、298K条件下,2mol氢气燃烧生成水蒸气放出484kJ热量,下列热化学方程式正确的是 | |
A. |
H2O(g)=H2(g)+ |
B. |
2H2(g)+O2(g)+2H2O(l); |
C. |
H2(g)+ |
D. |
2H2(g)+O2(g)=2H2O(g); |
|
下列离子方程式正确的是 | |
A. |
硫酸铝溶液中加过量氨水:Al3++4OH-=AlO2-+2H2O |
B. |
向硅酸钠溶液中通入过量的CO2:SiO32-+2CO2+2H2O=H2SiO3↓+2HCO3- |
C. |
过量铁粉与一定量稀硝酸反应:Fe+4H++NO3-=Fe3++NO↑+2H2O |
D. |
向NH4HSO4稀溶液中逐滴加入Ba(OH)2稀溶液至刚好沉淀完全: Ba2++2OH-+NH4++H++SO42-=BaSO4↓+NH3·H2O+H2O |
|
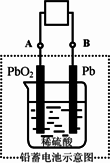
电瓶车所用电池一般为铅蓄电池,这是一种典型的可充电电池,电池总反应式为:Pb+PbO2+4H++2SO42-
| |
A. |
放电时:电子流动方向由B到A |
B. |
放电时:正极反应是Pb-2e-+SO42- |
C. |
充电时:铅蓄电池的负极应与充电器电源的正极相连 |
D. |
充电时:阳极反应是PbSO4-2e-+2H2O |
|
下列叙述正确的是 | |
A. |
0.01mol/LCH3COOH与pH=12的NaOH溶液混合,若有c(CH3COO-)>c(Na+),则混合液一定呈碱性 |
B. |
常温下,将等体积0.01mol/LHCl与pH=12的氨水混合,则混合液的pH=7, |
C. |
0.1mol/L的某二元弱酸盐Na2A溶液中,c(Na+)=2c(H2A)+2c(HA-)+2c(A2-) |
D. |
将5mL0.02mol/L的H2SO4与5mL0.02mol/LNaOH溶液充分混合,若混合后溶液的体积为10mL,则混合液的pH=2 |
|
下列各组离子,在指定的环境中一定能大量共存的是 | |
A. |
在pH为7的溶液中:Ag+、K+、SO42—、Cl— |
B. |
在能使pH试纸变深蓝色的溶液中:Na+、S2—、NO3—、CO32— |
C. |
在加入铝粉能产生H2的溶液中:NH4+、Fe2+、SO42—、NO3—、 |
D. |
在由水电离出的c(OH—)=10—13mol·L—1的溶液中:Na+、Ba2+、Cl—、I— |
|
合成氨工业对国民经济和社会发展具有重要的意义.哈伯法合成氨需要在20-50MPa的高压和500℃的高温下,并用铁作为催化剂,氨的转化率为10%-15%最近美国俄勒冈大学的化学家使用了一种名为trans-Fe(DMeOPrPE)2的催化剂,在常温下合成出氨,反应方程式可表示为N2+3H2——→2NH3,有关说法正确的是 | |
A. |
哈伯法合成氨是吸热反应,新法合成氨是放热反应 |
B. |
新法合成和哈伯法相比不需要在高温条件下,可节约大量能源,具有发展前景 |
C. |
新法合成能在常温下进行是因为不需要断裂化学键 |
D. |
新的催化剂降低了反应所需要的能量,提高了活化分子百分数 |
|
化学与数学有着密切的关系,将某些化学知识用数轴表示,可以收到直观形象、简明易记的效果.下列用数轴表示的化学知识中正确的是 | |
A. |
分散系的分类:
|
B. |
常温条件下,酚酞的变色范围:
|
C. |
HCl和NaAlO2溶液反应后铝元素的存在形式:
|
D. |
CO2通入澄清石灰水中反应的产物:
|