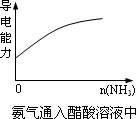
|
下列说法中正确的是 | |
A. |
NH3是极性分子,分子中N原子处在3个H原子所组成的三角形的中心 |
B. |
CCl4是非极性分子,分子中C原子处在4个Cl原子所组成的正方形的中心 |
C. |
H2O是极性分子,分子中O原子不处在2个H原子所连成的直线的中央 |
D. |
CO2是非极性分子,分子中C原子处在2个O原子所连成的直线的中央 |
|
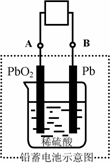
电瓶车所用电池一般为铅蓄电池,这是一种典型的可充电电池,电池总反应式为: Pb+PbO2+4H++2SO42- 则下列说法正确的是:
| |
A. |
放电时:电子流动方向由B到A |
B. |
放电时:正极反应是Pb-2e-+SO42- |
C. |
充电时:铅蓄电池的负极应与充电器电源的正极相连 |
D. |
充电时:阳极反应是PbSO4-2e-+2H2O |
|
下列反应的离子方程式正确的是 | |
A. |
Fe3O4与稀硝酸反应:Fe3O4+8H+ |
B. |
向硝酸银溶液中逐滴滴入稀氨水直至过量:Ag++2NH3·H2O |
C. |
含等物质的量的NaHCO3和Ba(OH)2溶液混合: HCO3-+Ba2++OH-=BaCO3↓+H2O |
D. |
Na2S溶液呈碱性:S2-+2H2O |
|
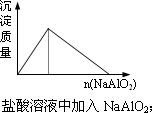
混合下列各组物质使之充分反应,加热蒸干产物并在300℃灼烧至质量不变,最终残留固体为纯净物的是 | |
A. |
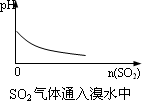
向亚硫酸钠溶液中滴加过量的溴水 |
B. |
将物质的量浓度相等的KAl(SO4)2与Ba(OH)2溶液以体积比1∶2混合 |
C. |
等体积、等物质的量浓度的碳酸钠与氢氧化钡溶液混合 |
D. |
在NaBr溶液中通入过量氯气 |
|
镁铁混合物4.9g,溶解在过量的稀硝酸中,完全反应得到标况下气体2.24L(假设气体全为NO),则向反应后的溶液中加入足量的烧碱,则可生成沉淀的量是 | |
A. |
6g |
B. |
8g |
C. |
10g |
D. |
12g |
|
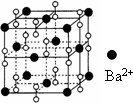
钡在氧气中燃烧时的得到一种钡的氧化物晶体,其结构如下图所示,有关说法正确的是
| |
A. |
该晶体属于离子晶体 |
B. |
晶体的化学式为Ba2O2 |
C. |
该晶体晶胞结构与CsCl相似 |
D. |
与每个Ba2+距离相等且最近的Ba2+共有12个 |
|
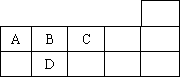
下表为元素周期表短周期的一部分,下列有关A、B、C、D四种元素的叙述不正确的是
| |
A. |
原子半径大小比较为D>B>C |
B. |
生成的氢化物分子间均可形成氢键 |
C. |
A与C形成的阴离子可能有AC32-、A2C42- |
D. |
A、B、C、D的单质常温下均不导电 |
|
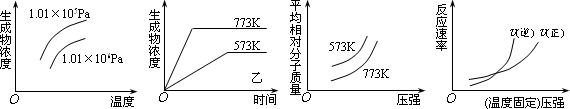
现有下列四个图像:
下列反应中全部符合上述图像的反应是 | |
A. |
N2(g)+3H2(g) |
B. |
2SO3(g) |
C. |
4NH3(g)+5O2(g) |
D. |
C(s)+CO2(g) |
|
下列离子方程式中正确的是 | |
A. |
向NaHCO3溶液中滴加少量澄清的石灰水: |
B. |
将NaOH固体加入浓的热的NH4Cl溶液: |
C. |
NaHS溶液呈碱性: |
D. |
向NaHSO4溶液中逐滴加入Ba(OH)2溶液至溶液呈中性
|