|
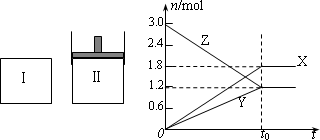
在一定温度下,将等量的气体分别通入起始体积相同的密闭容器Ⅰ和Ⅱ中,使其发生反应,t0时容器Ⅰ中达到化学平衡,X、Y、Z的物质的量的变化如图所示.则下列有关推断正确的是
| |
A. |
该反应的化学方程式为:3X+2Y |
B. |
若两容器中均达到平衡时,两容器的体积V(Ⅰ)<V(Ⅱ),则容器Ⅱ达到平衡所需时间大于t0 |
C. |
若两容器中均达到平衡时,两容器中Z的物质的量分数相同,则Y为固态或液态 |
D. |
若达平衡后,对容器Ⅱ升高温度时其体积增大,说明Z发生的反应为吸热反应 |
|
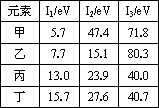
气态中性原子失去一个电子转化为气态正离子所需要的最低能量叫做第一电离能(I1),气态正离子继续失去电子所需最低能量依次称为第二电离能(I2)、第三电离能(I3)……下表是第三周期部分元素的电离能[单位:eV(电子伏特)]数据.
下列说法正确的是 | |
A. |
甲的金属性比乙强 |
B. |
乙的化合价为+1价 |
C. |
丙可能为非金属元素 |
D. |
丁一定是金属元素 |
|
设NA表示阿伏加德罗常数的值,下列叙述中正确的是 | |
A. |
常温常压下,8.8gCO2和N2O混合物中所含有的原子数为0.6NA |
B. |
Cu和足量的稀硝酸反应产生4.48L气体时,转移的电子数为0.6NA |
C. |
标准状况下,3.36L丁烷中含有的非极性键数为0.6NA |
D. |
在1L0.2mol/L的硫酸铁溶液中含有的硫酸根离子数为0.6NA |
|
将2.4gFe、Mg合金投入到一定量的稀硝酸中,金属与硝酸恰好完全反应,共收集到标准状况下的气体VL(硝酸被还原成NO),若向反应后的溶液中加入足量的NaOH溶液,待金属元素全部沉淀后,再将沉淀过滤、洗涤、灼烧后称量,质量为3.6g.则收集到的气体体积V值可为 | |
A. |
0.986 |
B. |
1.12 |
C. |
3.36 |
D. |
6.72 |
|
已知HF比CH3COOH易电离.关于物质的量浓度、体积都相同的NaF溶液和CH3COONa溶液,下列说法正确的是 | |
A. |
CH3COONa溶液中:c(CH3COO-)>c(Na+)>c(OH-)>c(H+) |
B. |
在相同条件下,两溶液的pH大小为:CH3COONa<NaF |
C. |
NaF溶液中:c(H+)+c(HF)=c(OH-) |
D. |
两溶液相比较,NaF溶液中的离子总数较多 |
|
将某些化学知识用数轴表示,可以收到直观、简明、易记的效果.用数轴表示的下列化学知识正确的是 | |
A. |
常温条件下,酚酞的变色范围: |
B. |
分散系的分类: |
C. |
AlCl3溶液与NaOH溶液反应后铝元素的存在形式: |
D. |
CO2和NaOH溶液反应后的产物: |
|
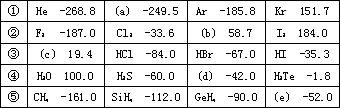
有五个系列同族元素的物质,101.3kP时测定它们的沸点(℃)如下表所示:
对应表中内容,下列叙述中正确的是 | |
A. |
a、b、c的化学式分别为Ne、Br2、HF |
B. |
系列②物质均有氧化性;系列③物质对应水溶液均是强酸 |
C. |
系列④中各化合物的稳定性顺序为:H20>H2S>H2Se>H2Te |
D. |
上表内物质HF和H2O,由于氢键的影响,其分子特别稳定 |