|
下列实验操作中错误的是 | |
A. |
分液时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 |
B. |
蒸馏时,应使温度计水银球靠近蒸烧瓶支管口 |
C. |
滴定时,左手控制滴定管活塞,右手握持锥形瓶,边滴边振荡,眼睛注视滴定管中的液面 |
D. |
称量时,称量物放在称量纸上,置于托盘天平的左盘,砝码放在托盘天平的右盘中 |
| |||||||||||||||||||||||||||||||||||||||
|
恒温恒容下,往一真空密闭容器中通入一定量的气体A,发生如下反应:2A(g) | |
A. |
若x=1,则p>a |
B. |
若x=2,则p<a |
C. |
若x=3,则p=a |
D. |
若x=4,则p≥a |
|
下列反应的离子方程式错误的是 | |
A. |
等物质的量的Ba(OH)2与NH4HSO4在稀溶液中反应: Ba2++2OH?/SUP>+2H++SO42?/SUP>=BaSO4↓+2H2O |
B. |
氢氧化铁与足量的氢溴酸溶液反应:Fe(OH)3+3H+=Fe3++3H2O |
C. |
足量的CO2通入饱和碳酸钠溶液中:CO2+2Na++CO32?/SUP>+H2O=2NaHCO3↓ |
D. |
向碳酸氢钠溶液中滴入过量澄清石灰水:Ca2++2OH?/SUP>+2HCO3?/SUP>=CaCO3↓+CO32?/SUP>+2H2O |
|
根据热化学方程式:S(s)+O2(g)=SO2(g);△H=-297.23kJ/mol,分析下列说法中正确的是 | |
A. |
S(g)+O2(g)=SO2(g);△H=-QkJ/mol.Q的值大于297.23 |
B. |
S(g)+O2(g)=SO2(g);△H=-QkJ/mol.Q的值小于297.23 |
C. |
1molSO2的总能量小于1molS和1molO2能量总和 |
D. |
1molSO2的总能量大于1molS和1molO2能量总和 |
|
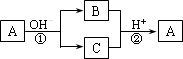
A是一种常见的单质,B、C为中学常见的化合物,A、B、C均含有元素X.它们有如下的转化关系(部分产物及反应条件已略去):
下列判断正确的是 | |
A. |
X元素可能为Al |
B. |
X元素一定为非金属元素 |
C. |
反应①和②互为可逆反应 |
D. |
反应①和②一定为氧化还原反应 |
|
设NA表示阿伏加德罗常数的值,下列叙述中正确的是 | |
A. |
常温常压下,8.8gCO2和N2O混合物中所含有的原子数为0.6NA |
B. |
Cu和足量的稀硝酸反应产生4.48L气体时,转移的电子数为0.6NA |
C. |
标准状况下,3.36L丁烷中含有的非极性键数为0.6NA |
D. |
在1L0.2mol/L的硫酸铁溶液中含有的硫酸根离子数为0.6NA |
|
一定条件下CuS与稀HNO3发生反应,所得还原产物为NO,氧化产物为SO42?/SUP>.现将0.06molCuS加入到50mL4.2mol/LHNO3中,充分反应之后,忽略溶液体积变化,下列说法正确的是 | |
A. |
被还原的硝酸为0.16mol |
B. |
反应后溶液中仍有硝酸剩余 |
C. |
反应后溶液的pH=1 |
D. |
CuS未全部参加反应 |
|
阿伏加德罗常数约为6.02×1023 mol-1,下列叙述中不正确的是 | |
A. |
将162.5g FeCl3转化为氢氧化铁胶体后,氢氧化铁胶体粒子数小于6.02×1023 |
B. |
在含196g H2SO4的浓硫酸溶液中加入足量的锌粉使其充分反应,则反应结束时,转移电子数约为4×6.02×1023 |
C. |
在石墨晶体中,平均0.3 mol碳碳共价键所含有的碳原子数约为 |
D. |
1mol C10H22分子中共价键总数约为31×6.02×1023 |