|
将一定量的氯气通入30 mL浓度为10.00 mol/L的氢氧化钠浓溶液中,加热少许时间后溶液中形成NaCl、NaClO、NaClO3共存体系.下列判断正确的是 | |
A. |
与NaOH反应的氯气一定为0.15 mol |
B. |
n(Na+)∶n(Cl-)可能为7∶3 |
C. |
若反应中转移的电子为n mol,则0.15<n<0.25 |
D. |
n(NaCl)∶n(NaClO)∶n(NaClO3)可能为11∶2∶1 |
|
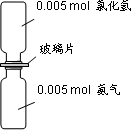
下图是氨气与氯化氢反应的装置.抽走玻璃片充分反应,反应中有关物理量的描述正确的是(NA表示阿伏加德罗常数)
| |
A. |
气体反应物的总体积为0.224 L |
B. |
生成物的分子个数为0.005 NA |
C. |
产物中的N- H键个数为0.02NA |
D. |
加水溶解后所得溶液中NH4+数目为0.005 NA |
|
化学反应中,有时存在“一种物质过量,另一种物质仍不能完全反应”的情况.下列反应中属于这种情况的是 | |
A. |
过量的MnO2与浓盐酸反应 |
B. |
过量的Zn与18 mol/L的硫酸反应 |
C. |
过量的Br2与FeI2反应 |
D. |
过量的H2与N2在催化剂存在下反应 |
|
将78 g金属钾在空气中燃烧,生成KO2和K2O2的混合物.该混合物与足量的CO2充分反应后生成O2(4KO2+2CO2→2K2CO3+3O2),得到O2的物质的量可能为 | |
A. |
0.50 mol |
B. |
0.75 mol |
C. |
1.00 mol |
D. |
1.50 mol |
|
碳酸有两个电离常数Ki1、Ki2,分别对应碳酸的两步电离.关于Ki1和Ki2说法正确的是 | |
A. |
Ki1的表达式为 |
B. |
Ki2对应的电离过程是HCO3-+H2O |
C. |
当碳酸的电离平衡正向移动时,Ki1与Ki2均相应增大 |
D. |
改变条件使Ki1减小,则Ki2一定也减小 |
|
将0.02 mol铜片溶于100 mL 9 mol/L HNO3中,产生336 mL气体(只含NO、NO2).该气体与一定量O2混合后,用一定量NaOH溶液完全吸收并恰好全部生成盐,则通入的O2体积可能为(气体体积均为标准状况) | |
A. |
11.2 mL |
B. |
22.4 mL |
C. |
56.2 mL |
D. |
67.2 mL |