|
下列说法正确的是 | |
A. |
常温下,反应4Fe(s)+3O2(g) |
B. |
CH3COOH |
C. |
氯碱工业中Cl2在阳极生成,该极同时还生成NaOH溶液 |
D. |
合成氨工业中采用高压的原因除增大原料的转化率外,还可加快反应速率 |
|
下列说法正确的是 | |
A. |
ΔH>0的反应,常温下一定不能自发进行 |
B. |
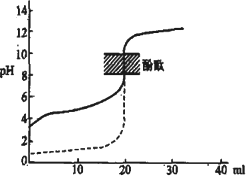
用0.1 mol/L NaOH溶液分别滴定相同物质的量浓度和相同体积的盐酸和醋酸,其中实线表示的是滴定盐酸的曲线
|
C. |
常温下,在0.1 mol/L氨水中,加入少量NH4Cl晶体,溶液的pH减小 |
D. |
恒容密闭容器中进行的反应3A(g) |
|
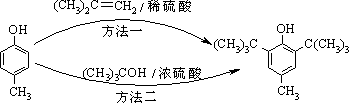
BHT(Butylated Hydroxy Toluene)是一种常用的食品抗氧化剂,合成方法有如下两种:
下列说法正确的是 | |
A. |
|
B. |
|
C. |
BHT久置于空气中会被氧化 |
D. |
两种方法的反应类型都是加成反应 |
|
将3.52 g CO2和SO2混合气体通入一定量的NaOH溶液中,气体全部与NaOH反应生成盐,将反应后的溶液减压低温蒸干后得到不含结晶水的固体,固体的质量可能为 | |
A. |
8.48 g |
B. |
7.48 g |
C. |
5.72 g |
D. |
5.22 g |
|
设NA为阿伏加德罗常数,下列说法中正确的是 | |
A. |
标准状况下,密度为d g/L的某气体纯净物一个分子的质量为 |
B. |
常温常压下,17 g甲基(-14CH3)所含的中子数为9NA |
C. |
25℃时,1 L pH=13的NaOH溶液中含有NA个氢氧根离子 |
D. |
4.6 g Na在空气中完全反应生成Na2O、Na2O2,转移0.2NA个电子 |
|
根据下表(部分短周期元素的原子半径及主要化合价)信息,判断以下叙述正确的是
| |
A. |
最高价氧化物对应水化物的碱性A>C |
B. |
氢化物的沸点H2D<H2E |
C. |
单质与稀盐酸反应的速率A<B |
D. |
C2+与A+的核外电子数相等 |
|
将一定量的H2、CO和CO2的混合气体通入盛有足量Na2O2粉末(Na2O2体积忽略不计)的密闭容器中,用电火花引燃直至反应完全.恢复到原温度,容器内的压强为原来的1/4,则原混合气体的平均相对分子质量不可能是 | |
A. |
15 |
B. |
28 |
C. |
30 |
D. |
36 |
|
能正确表示下列各组溶液混合后,所得液体恰好呈中性的离子方程式是 | |
A. |
Ba(OH)2和NaHSO4:Ba2++2OH-+2H++SO42-→BaSO4↓+2H2O |
B. |
Ba(OH)2和NaHSO4:Ba2++OH-+H++SO42-→BaSO4↓+H2O |
C. |
Ba(OH)2和KAl(SO4)2:2Ba2++4OH-+Al3++2SO42-→2BaSO4↓+AlO2- |
D. |
Ba(OH)2和KAl(SO4)2:3Ba2++6OH-+2Al3++3SO42-→3BaSO4↓+2Al(OH)3↓ |
|
三氟化氮(NF3)是微电子工业中优良的等离子刻蚀气体,它在潮湿的环境中能发生如下反应:3NF3+5H2O→2NO+HNO3+9HF.下列有关该反应的说法正确的是 | |
A. |
NF3是氧化剂,H2O是还原剂 |
B. |
NF3是极性分子,在潮湿空气中泄漏会看到红棕色气体 |
C. |
若生成1 mol HNO3,则转移2NA个电子 |
D. |
每消耗0.2 mol氧化剂,可收集到5.418 L气体 |
 (BHT)
(BHT)