|
实验室需用480 mL 0.1 mol/L的硫酸铜溶液,现选取500 mL容量瓶进行配制,以下操作正确的 | |
A. |
称取7.68克硫酸铜,加入500毫升水 |
B. |
称取12.0克胆矾配成500毫升溶液 |
C. |
称取8.0克硫酸铜,加入500毫升水 |
D. |
称取12.5克胆矾配成500毫升溶液 |
|
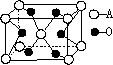
过渡元素的化合物是高温超导物质研究的热点.某过渡元素A与氧形成的化合物叫金红石,其晶体的最小结构单元如图.则下面有关金红石的说法正确的是
| |
A. |
一定是共价化合物 |
B. |
可能是离子化合物 |
C. |
它的化学式为AO2 |
D. |
它的化学式为A3O2 |
|
美国Lawtcce Lirermre国家实验室的V·Lota·C·S·Yoo和H·Cynn成功地在高压下将CO2转化为具有类似SiO2结构的原子晶体,下列关于CO2原子晶体的说法正确是 | |
A. |
CO2的原子晶体和分子晶体互为同素异形体 |
B. |
在一定条件下,CO2原子晶体转化为分子晶体是化学变化 |
C. |
CO2的原子晶体和CO2分子晶体具有相同的物理性质 |
D. |
CO2的原子晶体中,每个碳周围结合4个氧原子,每一个氧原子跟两个碳原子相结合 |
|
短周期元素A、B、C、D的原子序数依次增大,它们的原子序数之和为36,且原子最外层电子数之和为14;A、C原子的最外层电子数之和等于B原子的次外层电子;A与C,B与D均为同主族元素.下列叙述正确的是 | |
A. |
在地壳中,B元素的含量位于第二位 |
B. |
A、B、D三种元素形成的化合物一定是强酸 |
C. |
A元素与C元素形成的化合物与水反应后,溶液呈碱性 |
D. |
B元素与C元素形成的化合物C2B和C2B2中阴、阳离子个数比均为1∶2 |
|
香豆素是应用广泛的一种香料,它可以用水杨醛作原料合成.
| |
A. |
水杨醛和香豆素分子中均不含手性碳原子 |
B. |
水杨醛和香豆素分子中所有原子一定共平面 |
C. |
水杨醛和香豆素均能与溴水反应 |
D. |
水杨醛和香豆素各1 mol分别与足量的NaOH溶液反应,消耗NaOH的物质的量相等 |
|
下列说法正确的是 | |
A. |
在漂白粉中滴入70%的硫酸,立刻产生黄绿色气体,说明硫酸具有还原性 |
B. |
粗锌与稀硫酸反应比纯锌快,说明粗锌反应时形成了原电池 |
C. |
向滴有酚酞的Na2CO3溶液中滴加BaCl2溶液,红色变浅,说明BaCl2溶液有酸性 |
D. |
pH相同的两种一元酸HA溶液和HB溶液与足量Zn反应,HA比HB反应速率快,说明HA酸性更强 |
|
下列实验正确的是 | |
A. |
向沸腾的NaOH稀溶液中滴加FeCl3饱和溶液,制取Fe(OH)3胶体 |
B. |
苯酚沾到皮肤上,先用酒精清洗,再用水冲洗 |
C. |
将10 g ZnSO4·7H2O溶解在90 g水中,配制10% ZnSO4溶液 |
D. |
向稀硫酸中加几滴CuSO4溶液,可提高纯锌与稀硫酸的反应速率 |
|
对0.1 mol·L-1 NH4Cl溶液,下列分析正确的是 | |
A. |
c(Cl-)>c(NH |
B. |
c(NH |
C. |
适当加热该溶液后,水的离子积KW增大 |
D. |
加水稀释后溶液的pH减小 |
|
下列离子方程式正确的是 | |
A. |
NaHCO3溶液显碱性:HCO3-+H2O |
B. |
KOH溶液吸收少量SO2:2OH-+SO2 |
C. |
Na2O2与H2O反应制备O2:2Na2O2+2H2O |
D. |
碳酸钠溶液吸收少量醋酸:CO32-+H+ |

 H3O++CO32-
H3O++CO32- H2O+SO32-
H2O+SO32- 4Na++4OH-+O2↑
4Na++4OH-+O2↑ HCO3-
HCO3-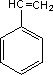 的分子式是C8H9
的分子式是C8H9