|
用NA表示阿伏加德罗常数的值.下列叙述正确的是 | |
A. |
常温常压下的33.6 L氯气与27 g铝充分反应,转移电子数为3 NA |
B. |
标准状况下,22.4 L己烷中共价键数目为19 NA |
C. |
由CO2和O2组成的混合物中共有NA个分子,其中的氧原子数为2 NA |
D. |
1 L浓度为1 mol·L-1的Na2CO3溶液中含有NA个CO32- |
|
有一定量的14%KOH溶液,加热蒸发掉100 g水后,变为80 mL 28%的KOH溶液,此时溶液的物质的量浓度为 | |
A. |
5 mol/L |
B. |
6 mol/L |
C. |
6.25 mol/L |
D. |
6.75 mol/L |
|
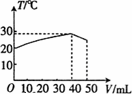
向盛有50 mL 1.00 mol·L-1 HC1溶液的绝热容器中加入NaOH溶液,NaOH溶液的体积(V)与所得混合溶液的最高测量温度(T)的关系如图所示,下列叙述中不正确的是
| |
A. |
该实验表明化学能可以转化为热能 |
B. |
NaOH溶液的浓度大于1.00 mol·L-1 |
C. |
V=50 mL时,混合液的pH>7 |
D. |
该实验表明有水生成的反应都是放热反应 |
|
下列所得溶液的物质的量浓度等于0.1 mol·L-1的是 | |
A. |
将0.1 mol氨充分溶解在1 L水中 |
B. |
将10 g质量分数为98%的硫酸与990 g水混合 |
C. |
将8 g三氧化硫溶于水并配成1 L溶液 |
D. |
将0.1 mol氧化钠溶于水并配成1 L溶液 |
|
设NA这阿伏加德罗常数的数值,下列有关叙述中不正确的是 | |
A. |
Na2O2与H2O反应生成1.12 L(标准状况下)O2,反应中转移的电子数为0.1 NA |
B. |
常温常压下,NA个甲烷分子的体积大于22.4 L |
C. |
0.1 mol·L-1的NaHSO4溶液中含0.2 NA个阳离子 |
D. |
121 g CC12F2中含氟原子的个数为2 NA |
|
阿伏加德罗常数约为6.02×1023 mol-1,下列叙述中正确的是 | |
A. |
常温常压下,18.0 g重水(D2O)所含的电子数约为10×6.02×1023 |
B. |
室温下,42.0 g乙烯和丙烯的混合气体中含有的碳原子数约为3×6.02×1023 |
C. |
标准状况下,22.4 L甲苯所含的分子数约为6.02×1023 |
D. |
标准状况下,a L甲烷和乙烷混合气体中的分子数约为 |
|
铜与1 mol/L的硝酸反应,如果 | |
A. |
0.2 mol·L-1 |
B. |
0.4 mol·L-1 |
C. |
0.6 mol·L-1 |
D. |
0.8 mol·L-1 |
|
下列说法正确的是 | |
A. |
把100 mL 3 mol·L-1的H2SO4跟100 mL H2O混合,硫酸的物质的量浓度改变为1.5 mol·L-1 |
B. |
把100 g 20%的NaCl溶液跟100 g H2O混合后,NaCl溶液的质量分数是10% |
C. |
把200 mL 3 mol·L-1的BaCl2溶液跟100 mL 3 mol·L-1的KCl溶液混合后,溶液中的C(Cl-)仍然是3 mol·L-1 |
D. |
把100 mL 20%的NaOH溶液跟100 mL H2O混合后,NaOH溶液的质量分数是10% |
|
在三个密闭容器中分别充入Ne、H2、O2三种气体,当他们的温度和密度都相同时,这三种气体的压强(p)由大到小的顺序是 | |
A. |
p(Ne)>p(H2)>p(O2) |
B. |
p(O2)>p(Ne)>p(H2) |
C. |
p(H2)>p(O2)>p(Ne) |
D. |
p(H2)>p(Ne)>p(O2) |