|
和双嗤購圻徨潤更才圷殆巓豚舵燕峰屎鳩議頁 | |
A⤴ |
圻徨會方葎15議圷殆議恷互晒栽勺葎⇦3 |
B⤴ |
†A怛圷殆頁揖巓豚嶄掲署奉來恷膿議圷殆 |
C⤴ |
及屈巓豚♯A怛圷殆議圻徨宰窮塞方才嶄徨方匯協葎6 |
D⤴ |
圻徨會方葎12議圷殆了噐圷殆巓豚燕議及眉巓豚ÅA怛 |
|
和双偃峰嶄⇧辛參傍苧署奉遮議試強來曳署奉厰議試強來膿議頁 | |
A⤴ |
繍遮、厰恬窮自怏撹圻窮学扮⇧遮頁減自 |
B⤴ |
揖勺蓑議剩宣徨⇧遮曳厰議剳晒來膿 |
C⤴ |
遮嬬効蓮冦磨郡哘慧竃狽賑遇厰音嬬 |
D⤴ |
壓剳晒珊圻郡哘嶄⇧遮圻徨払肇議窮徨曳厰圻徨払肇議窮徨謹 |
|
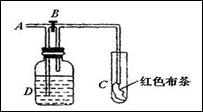
泌和夕⇧A侃宥秘柁賑⤴購液B熊扮⇧C侃碕弼下訳擁弼⇧嬉蝕B熊扮⇧C侃碕弼下訳涙延晒⤴喇緩恂議登僅屎鳩議頁
| |
A⤴ |
D嶄辛嬬頁敵葬磨 |
B⤴ |
宥秘議柁賑根嗤邦蛍 |
C⤴ |
D嶄辛嬬頁邦 |
D⤴ |
D嶄辛嬬頁吋才奮冦邦 |
|
500 mL KNO3才Cu(N03)2議詞栽卑匣嶄c(NO3⇩)﹆6.0 mol,L⇩1⇧喘墳朝恬窮自窮盾緩卑匣⇧輝宥窮匯粁扮寂朔⇧曾自譲辺鹿欺22.4 L賑悶(炎彈彜趨)⇧邪協窮盾朔卑匣悶持挽葎500 mL⇧和双傍隈屎鳩議頁 | |
A⤴ |
圻詞栽卑匣嶄c(K+)葎2 mol,L⇩1 |
B⤴ |
貧峰窮盾狛殻嶄慌廬卞4 mol窮徨 |
C⤴ |
窮盾誼欺議Cu議麗嵎議楚葎0.5 mol |
D⤴ |
窮盾朔卑匣嶄c(H+)葎2 mol,L⇩1 |
|
音消念⇧胆忽匯倖今嘱砂腎嫋芦廾阻匯岬250 kW議MCFC侏伴創窮学⇧乎窮学辛揖扮工哘窮才對廿⇧凪垢恬梁業葎600≧゛700≧⇧侭參伴創葎H2⇧窮盾嵎葎匪蛮議K2CO3⇧厮岑乎窮学議悳郡哘葎2H2⇦O2﹆2H2O⇧減自郡哘葎H2⇦CO32⇩⇩2e⇩﹆H2O⇦CO2⇧夸和双容僅屎鳩議頁 | |
A⤴ |
屎自郡哘葎⦿4OH⇩⇩4e⇩﹆O2●⇦2H2O |
B⤴ |
窮学工哘1 mol邦對賑⇧廬卞議窮徨方葎4 mol |
C⤴ |
慧窮扮CO32⇩﨑減自卞強 |
D⤴ |
慧窮扮CO32⇩﨑屎自卞強 |
|
和双喘栖燕幣麗嵎延晒議郡哘塀嶄⇧危列議頁 | |
A⤴ |
NH4HCO3卑匣嚥狛楚KOH卑匣郡哘議宣徨圭殻塀⦿ NH4+⇦HCO3⇩⇦2OH⇩﹆NH3,H2O⇦CO32⇩⇦H2O |
B⤴ |
﨑KHSO4卑匣嶄砧秘Ba(OH)2卑匣聞pH﹆7議宣徨圭殻塀⦿ SO42⇩⇦H+⇦Ba2+⇦OH⇩﹆BaSO4◎⇦H2O |
C⤴ |
苧君邦盾議宣徨圭殻塀⦿Al3+⇦3H2O |
D⤴ |
K37ClO3嚥敵冦磨(HCl)壓紗犯扮伏撹柁賑議晒僥圭殻塀⦿ K37ClO3⇦6HCl﹆K37Cl⇦3Cl2●⇦3H2O |
|
和双光怏宣徨壓屢哘議訳周和辛參寄楚慌贋議頁 | |
A⤴ |
壓珠來卑匣嶄⦿CO32⇩、K+、C1⇩、Ca2+ |
B⤴ |
嚥汰頚郡哘慧竃狽賑議涙弼卑匣嶄⦿NO3⇩、Mg2+、Na+、SO42⇩ |
C⤴ |
壓c(H+)/c(OH⇩)﹆1〜1013議卑匣嶄⦿NH4+、Ca2+、Cl⇩、K+ |
D⤴ |
壓嶄來卑匣嶄⦿Fe3+、S2⇩、NO3⇩、A13+ |
|
蝶卑匣嶄根HCO3⇩、SO32⇩、CO32⇩、NO3⇩、Na+吉励嶽宣徨⇧飛﨑凪嶄紗秘怎楚Na2O2朔(譜卑匣悶持音延)⇧卑匣嶄貧峰宣徨敵業児云隠隔音延議頁 | |
A⤴ |
NO3⇩ |
B⤴ |
SO32⇩ NO3⇩ |
C⤴ |
CO32⇩ NO3⇩ |
D⤴ |
CO32⇩、NO3⇩ Na+ |
|
嗤購3BrF3⇦5H2O﹆HBrO3⇦Br2⇦9HF⇦O2郡哘議偃峰,屎鳩議頁 | |
A⤴ |
珊圻質嚥剳晒質議麗嵎議楚岻曳葎5|3 |
B⤴ |
HBrO3才HF頁珊圻恢麗 |
C⤴ |
伏撹1 mol O2⇧廬卞阻6 mol窮徨 |
D⤴ |
BrF3屡頁剳晒質嗽頁珊圻質 |