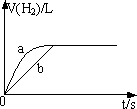|
设NA为阿伏加德罗常数.下列叙述正确的是 | |
A. |
常温下,11.2 L O2所含氧原子数为NA |
B. |
23 g Na在空气中完全燃烧,转移电子数为NA |
C. |
常温下,0.5 mol/L H2SO4中含H+数为NA |
D. |
46 g NO2和N2O4混合气体中含有原子数为3 NA |
|
某溶液中含有两种溶质H2SO4和NaCl,物质的量之比为1∶3,用铜作电极电解该溶液,下列叙述正确的是 | |
A. |
阴极产生的气体是H2 |
B. |
阳极先析出Cl2后析出O2 |
C. |
电解的最后阶段为电解水 |
D. |
阳极产生的Cl2的物质的量大于O2 |
|
已知1 mol N2(气态)与适量H2(气态)反应,生成NH3(气态),放出92 kJ的热量,且形成1 mol N-H键时放出391 kJ的热量,完全断裂1 mol H-H键吸收436 kJ的热量,则1 mol N2断键时吸收热量的 | |
A. |
946 kJ |
B. |
135 kJ |
C. |
1130 kJ |
D. |
780 kJ |
|
用惰性电极电解一定浓度的硫酸铜溶液,通电一段时间后,向所得溶液中加入0.4 mol氧化铜后恰好恢复至电解前的浓度.则电解过程中转移的电子数是 | |
A. |
1.6 mol |
B. |
1.2 mol |
C. |
0.8 mol |
D. |
0.4 mol |
|
已知热化学方程式2SO3(g) | |
A. |
a>197 |
B. |
a<197 |
C. |
a=197 |
D. |
热化学方程式中化学计量数表示分子个数 |
|
据报道,摩托罗拉公司研发一种由甲醇和氧气以及强碱做电解质溶液的新型手机电池,电量可达现在使用的镍氢电池或锂电池的十倍,可连续使用一个月才充一次电.其电池反应为:2CH3OH+3O2+4OH- | |
A. |
放电时CH3OH参与反应的电极为正极 |
B. |
充电时电解质溶液的pH逐渐增大 |
C. |
放电时负极的电极反应为:CH3OH-6e-+8OH-=CO32-+6H2O |
D. |
充电时每生成1 mol CH3OH转移6 mol电子 |
|
两种有机物以一定比例混合,一定条件下在aLO2(足量)燃烧,充分反应后恢复到原状态,再通过足量Na2O2层,得到气体仍是aL,下列混合有机物中符合此条件的是 | |
A. |
CH4,C2H4 |
B. |
CH3OH,CH3COOH |
C. |
C2H6,HCHO |
D. |
HCOOH,CH3COOCH3 |
|
一定质量的Na,K分别投入一定量的稀盐酸中,在相同条件下产生氢气的体积随时间变化的曲线如图中a,b所示,则下列说法中正确的是
| |
A. |
投入的Na,K物质的量一定相等 |
B. |
曲线a对应的反应使用了催化剂 |
C. |
曲线a代表K的反应,曲线b代表Na的反应, |
D. |
两反应中盐酸必须是足量 |
|
对于下列物质的量浓度相同的溶液,以下叙述正确的是 ①NaCl ②FeCl2 ③AlCl3 ④Na2CO3 ⑤NaHCO3 | |
A. |
都是无色溶液 |
B. |
②,③,⑤能使紫色石蕊试液变红 |
C. |
等体积等物质的量浓度的AgNO3溶液完全反应,需要①②③溶液的体积比为3∶2∶1 |
D. |
④,⑤都能和盐酸反应放出二氧化碳,从反应现象看,⑤和盐酸反应速率更快 |
|
已知工业上真空炼铷的原理如下:2RbCl+Mg | |
A. |
铷的金属活动性不如镁强,故镁可置换铷 |
B. |
铷的沸点比镁低,把铷蒸气抽出时,平衡右移 |
C. |
MgCl2的热稳定性不如RbCl强 |
D. |
铷的单质状态较化合物状态更稳定 |