|
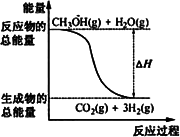
甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理是 ①CH3OH(g)+H2O(g)=CO2(g)+3H2(g);ΔH=+49.0 kJ·mol-1 ②CH3OH(g)+1/2O2(g)=CO2(g)+2H2(g);ΔH=-192.9 kJ·mol-1 下列说法正确的是 | |
A. |
CH3OH的燃烧热为192.9 kJ·mol-1 |
B. |
反应①中的能量变化如图所示
|
C. |
CH3OH转变成H2的过程一定要吸收能量 |
D. |
根据②推知反应CH3OH(l)+1/2O2(g)=CO2(g)+2H2(g)的ΔH>-192.9 kJ·mol-1 |
|
工业上制备纯硅反应的热化学方程式如下:SiCl4(g)+2H2(g)=Si(s)+4HCl(g);ΔH=+QkJ/mol(Q>0),某温度、压强下,将一定量反应物通入密闭容器进行以上反应(此条件下为可逆反应),下列叙述正确的是 | |
A. |
反应过程中,若压缩容器体积增大压强不能提高SiCl4的转化率 |
B. |
若反应开始时SiCl4为1 mol,则达平衡时,吸收热量为QkJ |
C. |
反应至4 min时,若HCl浓度为0.12 mol/L,则H2的反应速率为0.03 mol/(L·min) |
D. |
当反应吸收热量为0.025 QkJ时,生成的HCl通入100 mL 1 mol/L的NaOH溶液恰好反应 |
|
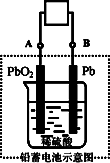
电瓶车所用电池一般为铅蓄电池,这是一种典型的可充电电池,电池总反应式为:Pb+PbO2+4H++2SO42-
| |
A. |
放电时:电子流动方向由A到B |
B. |
放电时:正极反应是Pb-2e-+SO42- |
C. |
充电时:铅蓄电池的负极应与充电器电源的正极相连 |
D. |
充电时:阳极反应是PbSO4-2e-+2H2O |
|
下列说法中,不正确的是 | |
A. |
电解精炼铜时,粗铜中的金、银、锌等形成阳极泥而与铜分离 |
B. |
在海轮外壳连接锌块保护外壳不受腐蚀是采用了牺牲阳极的阴极保护法 |
C. |
用铝质铆钉焊接铁板,铁不易被腐蚀 |
D. |
钢铁设备与外加直流电源的负极相连可以防止钢铁腐蚀 |
|
下列有关金属腐蚀与防护的说法正确的是 | |
A. |
当镀锡铁制品的镀层破损时,锡层仍能对铁制品起保护作用 |
B. |
纯银器表面在空气中渐渐变暗是因为发生了化学腐蚀 |
C. |
可将地下输油钢管与外加直流电源的正极相连以保护它不受腐蚀 |
D. |
在海轮外壳连接锌块保护外壳不受腐蚀是采用了牺牲阳极的阴极保护法 |
|
电池是人类生产和生活中的重要能量来源,各式各样电池的发展是化学对人类的一项重大贡献.下列有关电池的叙述正确的是 | |
A. |
锌锰干电池工作一段时间后碳棒变细 |
B. |
氢氧燃料电池可将热能直接转变为电能 |
C. |
氢氧燃料电池工作时氢气在负极被氧化 |
D. |
太阳能电池的主要材料是高纯度的二氧化硅 |