|
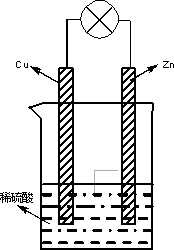
下列有关金属腐蚀与防护的说法正确的是 | |
A. |
纯银器表面在空气中因电化学腐蚀渐渐变暗 |
B. |
当镀锌铁制品的镀层破损时,镶层仍能对铁制品起保护作用 |
C. |
在海轮外壳连接锌块保护外壳不受腐蚀是采用了牺牲阳极的阴极保护法 |
D. |
可将地下输油钢管与外加直流电源的正极相连以保护它不受腐蚀 |
|
一定温度下,在固定容积、体积为2 L的密闭容器中充入1 mol N2和3 mol H2发生反应,当反应进行到10 s末时达到平衡,此时容器中c(NH3)=0.15 mol·L-1.下列有关判断正确的是 | |
A. |
反应达平衡时N2的转化率为7.5% |
B. |
反应进行到10 s末时,H2的平均反应速率是0.0225 mol·L-1·s-1 |
C. |
该反应达到平衡时的标志是容器中气体密度不再改变 |
D. |
再往该容器中充入1 mol N2和3 mol H2,重新达到平衡时c(NH3)>0.30 mol·L-1 |
|
2007年10月10日,德国科学家哈德·埃尔特生日当天获得了诺贝尔化学奖,以奖励他在表面化学领域做出开拓性的贡献.合成氨反应在铁催化剂表面进行时效率显著提高,就是埃尔特的研究结果,下列关于合成氨反应的叙述中正确的是 | |
A. |
铁做催化剂可加快反应速率,且有利于平衡向合成氨的方向移动 |
B. |
将氨气从混合气中分离,可加快反应速率,且有利于平衡向合成氨的方向移动 |
C. |
升高温度可加快反应速率,且有利于平衡向合成氨的方向移动 |
D. |
增大压强可加快反应速率,且有利于平衡向合成氨的方向移动 |
|
设NA代表阿伏加德罗常数的数值,下列说法中正确的是 ①常温常压下,17 g甲基(-14CH3)所含的中子数为9NA ②常温常压下,22.4 L NO气体的分子数小于NA ③64 g铜发生氧化还原反应,一定失去2NA个电子 ④常温常压下,100 mL 0.5 mol/L的乙酸溶液中,乙酸的分子数目小于0.05NA ⑤标准状况下,22.4 L二氯甲烷所含有的分子数为NA ⑥常温常压下,1 mol氦气含有的核外电子数为4NA | |
| [ ] | |
A. |
①② |
B. |
③④ |
C. |
②④ |
D. |
⑤⑥ |
|
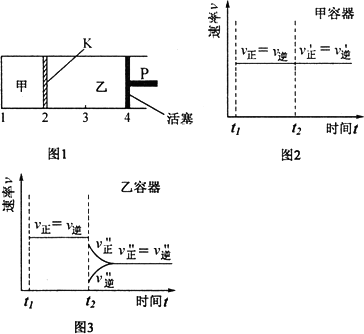
一定温度下可逆反应:A(s)+2B(g)
| |
| [ ] | |
A. |
保持温度和活塞P位置不变,在甲中再加入1 mol A和2 mol B,达到新的平衡后,甲中C的浓度是乙中C的浓度的2倍 |
B. |
保持活塞P位置不变,升高温度,达到新的平衡后,K会向右移动 |
C. |
保持温度和K位置不变,移动活塞P,使乙的容积和甲相等,达到新的平衡后,乙中C的体积分数小于甲中C的体积分数 |
D. |
保持温度和乙中的压强不变,t2时分别向甲、乙中加入等质量的氦气后,甲、乙中反应速率变化情况分别如图2和图3所示(t1前的反应速率变化已省略) |
|
将含有O2和CH4的混合气体置于盛有23.4 g Na2O2的密闭容器中,电火花点燃,反应结束后,容器内的压强为零(150℃),将残留物溶于水中,无气体产生.下列叙述正确的是 | |
| [ ] | |
A. |
原混合气体中O2和CH4的体积比为2∶1 |
B. |
残留物只有Na2CO3 |
C. |
原混合气体中O2与CH4的体积比为1∶2 |
D. |
原混合气体的密度是在同温同压下氢气密度的15倍 |