|
甲酸和乙酸都是弱酸,当它们的浓度均为0.10 mol·L-1时,甲酸中的c(H+)约为乙酸中c(H+)的3倍.现有两种浓度不等的甲酸溶液a和b,以及0.10 mol·L-1的乙酸,经测定它们的pH从大到小依次为a、乙酸、b.由此可知 | |
| [ ] | |
A. |
a的浓度必小于乙酸的浓度 |
B. |
a的浓度必大于乙酸的浓度 |
C. |
b的浓度必小于乙酸的浓度 |
D. |
b的浓度必大于乙酸的浓度 |
|
等物质的量的N2、O2、CO2混合气体通过Na2O2后,体积变为原体积的8/9(同温同压),这时混合气体中N2、O2、CO2物质的量之比为 | |
| [ ] | |
A. |
3∶4∶1 |
B. |
3∶3∶2 |
C. |
6∶7∶3 |
D. |
6∶9∶0 |
|
CuS和Cu2S都能溶于硝酸,它们高温灼烧的产物相同,以下鉴别CuS和Cu2S两种黑色粉末的方法合理的是 | |
| [ ] | |
A. |
将两种样品分别溶于硝酸,区别所产生的气体 |
B. |
将两种样品分别溶于硝酸,区别溶液的颜色 |
C. |
取两种同质量的样品分别在高温灼烧,区别残留固体的质量 |
D. |
取两种同质量的样品分别在高温灼烧,区别残留固体的颜色 |
|
将标准状况下的2.24 L CO2通入150 mL 1 mol/L NaOH溶液中,下列说法正确的是 | |
| [ ] | |
A. |
c(HCO3-)略大于c(CO32-) |
B. |
能使酸性高锰酸钾溶液褪色 |
C. |
c(Na+)等于c(CO32-)与c(HCO3-)之和 |
D. |
c(HCO3-)略小于c(CO32-) |
|
X、Y、Z是原子序数依次增大且属于不同周期的三种常见短周期元素,三种元素相互之间可以形成1∶1型的化合物M、N、R,常温下M、N为固体,R为液体.M、N遇到水都能产生气体,而且产生的气体相互可以化合,下列说法正确的是 | |
| [ ] | |
A. |
三种元素都是非金属元素 |
B. |
Z是地壳中含量最多的元素 |
C. |
三种化合物都是共价化合物 |
D. |
M、N投入水中所得溶液中溶质相同 |
|
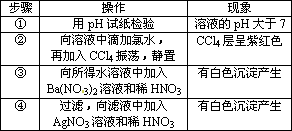
某无色溶液中只可能含有①Na+、②Ba2+、③Cl一、④I一、⑤SO32一、⑥SO42一离子中的若干种(忽略水电离出的H+、OH一),依次进行下列实验,且每步所加试剂均过量,观察到现象如下表.下列结论正确的是
| |
| [ ] | |
A. |
肯定含有的离子是③④⑤ |
B. |
肯定没有的离子是②⑤ |
C. |
可能含有的离子是①⑥ |
D. |
不能确定的离子是③⑥ |
|
向10 mL 0.1 mol/L NH4Al(SO4)2溶液中,滴加等浓度Ba(OH)2溶液x mL,下列叙述正确的 | |
| [ ] | |
A. |
x=10时,溶液中有NH4+、Al3+、SO42-,且c(NH4+)>c(Al3+) |
B. |
x=10时,溶液中有NH4+、AlO2-、SO42-,且c(NH4+)>c(SO42-) |
C. |
x=30时,溶液中有Ba2+、AlO2-、OH-,且c(OH-)<c(AlO2-) |
D. |
x=30时,溶液中有Ba2+、Al3+、OH-,且c(OH-)=c(Ba2+) |
|
我国化学家侯德榜根据在相同的温度下NaHCO3溶解度比NaCl、Na2CO3、NH4HCO3和NH4Cl的溶解度都小的性质,运用CO2+NH3+H2O+NaCl
则下列叙述正确的是 | |
| [ ] | |
A. |
A气体是CO2,B气体是NH3 |
B. |
第Ⅲ步得到的晶体是难溶于水的 |
C. |
第Ⅲ步操作用到的主要玻璃仪器是烧杯、漏斗、玻璃棒 |
D. |
第Ⅳ步操作的主要过程有溶解、蒸发、结晶 |
|
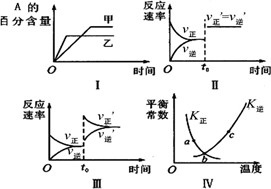
在密闭容器中进行反应:2A(g)+B(g)
| |
| [ ] | |
A. |
图Ⅰ表示温度对化学平衡的影响,且甲的温度较高 |
B. |
图Ⅱ表示t0时刻缩小容器体积对反应速率的影响 |
C. |
图Ⅲ表示t0时刻增大B浓度对反应速率的影响 |
D. |
图Ⅳ中a、b、c三点中只有b点已经达到化学平衡状态 |