|
下列叙述正确的是 | |
| [ ] | |
A. |
95℃纯水的pH<7,说明加热可导致水呈酸性 |
B. |
pH=3的醋酸溶液,稀释至10倍后pH=4 |
C. |
0.2 mol/L的盐酸,与等体积水混合后pH=1 |
D. |
pH=3的醋酸溶液,与pH=11的氢氧化钠溶液等体积混合后pH=7 |
|
几种短周期元素的原子半径及主要化合价见下表:
根据表中信息,判断以下说法正确的是 | |
| [ ] | |
A. |
单质与稀硫酸反应的速率快慢:R>Y>X |
B. |
离子半径:T2->X2+ |
C. |
元素最高价氧化物的水化物的碱性:Y>R>X |
D. |
单质与氢气化合的难易程度:Z>T |
|
某无色溶液中可能含有Na+、Fe2+、Br-、CO32-、I-、SO32-六种离子中的几种. ①在该溶液中滴加足量氯水后,有气泡产生、溶液呈橙黄色; ②向呈橙黄色的溶液中加入BaCl2溶液时无沉淀生成; ③向淀粉溶液中滴加橙黄色溶液未变蓝色.根据上述实验事实推断,在该溶液中肯定存在的离子组是 | |
| [ ] | |
A. |
Na+、I-、SO32- |
B. |
Fe2+、I-、SO32- |
C. |
Na+、Br-、CO32- |
D. |
Fe2+、Br-、CO32- |
|
下列化学反应的离子方程式不正确的是 | |
| [ ] | |
A. |
铁屑溶于过量稀硝酸:3Fe+8H++2NO3- |
B. |
Fe(OH)3溶于过量的HI溶液:2Fe(OH)3+6H++2I- |
C. |
在AlCl3溶液中加入过量氨水:Al3++3NH3·H2O |
D. |
过量的NaHSO4溶液与Ba(OH)2溶液反应:2H++SO42-+Ba2++2OH- |
|
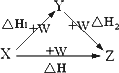
下图中,A是一种正盐,B是气态氢化物,C是单质,F是强酸.当X无论是强酸还是强碱时都有如下转化关系(其他反应产物及反应所需条件均已略去),当X是强碱时,过量的B跟Cl2反应除生成C外,另一产物是盐酸盐.
下列说法中不正确的是 | |
| [ ] | |
A. |
当X是强酸时,A、B、C、D、E、F中均含同一种元素,F可能是H2SO4 |
B. |
当X是强碱时,A、B、C、D、E、F中均含同一种元素,F是HNO3 |
C. |
B和Cl2的反应是氧化还原反应 |
D. |
当X是强酸时,C在常温下是气态单质 |
|
下列各组中的两种物质相互反应时,无论哪种过量,都可用同一个离子方程式表示的是 ①碳酸钠溶液与盐酸 ②硫化氢气体与氯化铁溶液 ③硫酸铝溶液与氨水 ④硝酸银溶液与氨水 ⑤碘化亚铁溶液与氯水 ⑥碳酸氢钙溶液与澄清石灰水 | |
| [ ] | |
A. |
③⑤ |
B. |
①③⑥ |
C. |
②④ |
D. |
②③⑥ |
|
将足量NO2通入下列各溶液中,所含离子还能大量共存的是 | |
| [ ] | |
A. |
Fe2+、CH3COO-、SO |
B. |
Ca2+、K+、Cl-、HCO |
C. |
NH |
D. |
K+、Na+、SO32-、AlO2- |
|
下列方程式书写正确的是 | |
| [ ] | |
A. |
CuSO4溶液与Ba(OH)2溶液混合:Cu2++SO42-+2OH-+Ba2+ |
B. |
NaHCO3水解的离子方程式:HCO3-+H2O |
C. |
K37ClO3与浓盐酸反应制氯气的化学方程式: K37ClO3+6HCl (浓) |
D. |
小苏打与氢氧化钠溶液混合:HCO3-+OH-=CO2↑+H2O |