|
已知反应:2SO2(g)+O2(g)
| |
| [ ] | |
A. |
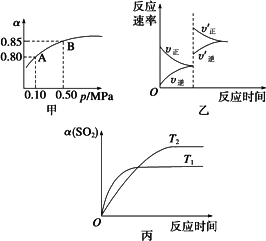
由图甲知,A点SO2的平衡浓度为0.4 mol/L |
B. |
由图甲知,B点SO2、O2、SO3的平衡浓度之比为2∶1∶2 |
C. |
达平衡后,缩小容器容积,则反应速率变化图象可以用图乙表示 |
D. |
压强为0.50 MPa时不同温度下SO2转化率与温度关系如丙图,则T2>T1 |
|
COCl2(g) | |
| [ ] | |
A. |
①②④ |
B. |
①④⑥ |
C. |
②③⑤ |
D. |
③⑤⑥ |
|
如图所示为装有活塞的密闭容器,内盛22.4 mL NO.若通入11.2 mL氧气(气体体积均在标准状况下测定),保持温度、压强不变,则容器内混合气体的密度为
| |
| [ ] | |
A. |
等于1.369 g/L |
B. |
等于2.054 g/L |
C. |
在1.369 g/L和2.054 g/L之间 |
D. |
大于2.054 g/L |
|
对已达到化学平衡的反应:2X(g)+Y(g) | |
| [ ] | |
A. |
逆反应速率增大,正反应速率减小,平衡向逆反应方向移动 |
B. |
逆反应速率减小,正反应速率增大,平衡向正反应方向移动 |
C. |
正、逆反应速率都减小,平衡向逆反应方向移动 |
D. |
正、逆反应速率都增大,平衡向正反应方向移动 |
|
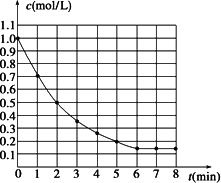
下图表示反应X(g)
下列有关该反应的描述正确的是 | |
| [ ] | |
A. |
第6 min后,反应就终止了 |
B. |
X的平衡转化率为85% |
C. |
若升高温度,X的平衡转化率将大于85% |
D. |
若降低温度,v正和v逆将以同样倍数减小 |
|
在恒容密闭容器中A(g)+3B(g) | |
| [ ] | |
A. |
容器中混合气体的平均相对分子质量增大 |
B. |
正反应速率增大,逆反应速率减小,平衡向正反应方向移动 |
C. |
正反应速率和逆反应速率都变小,C的百分含量增加 |
D. |
混合气体密度的变化情况不可以作为判断反应是否再次达平衡的依据 |
|
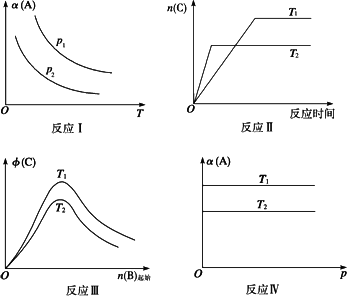
某化学科研小组研究在其他条件不变时,改变某一条件对反应[可用aA(g)+bB(g)
| |
| [ ] | |
A. |
反应Ⅰ:若p1>p2,则此反应只能在高温下自发进行 |
B. |
反应Ⅱ:此反应的ΔH<0,且T1<T2 |
C. |
反应Ⅲ:ΔH>0且T2>T1或ΔH<0且T2<T1 |
D. |
反应Ⅳ:T1<T2,则该反应不易自发进行 |
|
在一体积可变的密闭容器中,加入一定量的X、Y,发生反应mX(g)??nY(g);ΔH=Q kJ/mol.反应达到平衡时,Y的物质的量浓度与温度、气体体积的关系如下表所示:
下列说法正确的是 | |
| [ ] | |
A. |
m>n |
B. |
Q<0 |
C. |
温度不变,压强增大,Y的质量分数减少 |
D. |
体积不变,温度升高,平衡向逆反应方向移动 |
|
一定条件下,体积为10 L的密闭容器中,1 mol X和1 mol Y进行反应:2X(g)+Y(g) | |
| [ ] | |
A. |
以X浓度变化表示的反应速率为0.001 mol/(L·s) |
B. |
将容器体积变为20 L,Z的平衡浓度变为原来的 |
C. |
若增大压强,则物质Y的转化率减小 |
D. |
若升高温度,X的体积分数增大,则该反应的ΔH>0 |
|
密闭容器中进行下列反应:M(g)+N(g)
| |
| [ ] | |
A. |
正反应吸热,L为气体 |
B. |
正反应吸热,L为固体或纯液体 |
C. |
正反应放热,L为气体 |
D. |
正反应放热,L为固体或纯液体 |