|
25℃、101 kPa下,碳、氢气、甲烷和葡萄糖的燃烧热依次是393.5 kJ/mol、285.8 kJ/mol、890.3 kJ/mol、2800 kJ/mol,则下列热化学方程式正确的是 | |
| [ ] | |
A. |
C(s)+ |
B. |
2H2(g)+O2(g) |
C. |
CH4(g)+2O2(g) |
D. |
|
|
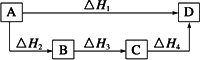
根据盖斯定律判断如下图所示的物质转变过程中,正确的等式是
| |
| [ ] | |
A. |
ΔH1=ΔH2=ΔH3=ΔH4 |
B. |
ΔH1+ΔH2=ΔH3+ΔH4 |
C. |
ΔH1+ΔH2+ΔH3=ΔH4 |
D. |
ΔH1=ΔH2+ΔH3+ΔH4 |
|
硒(Se)是人体必需的一种微量元素,其单质可用于制光敏电阻、复印机的硒鼓等等.工业上提取硒的方法之一是用硫酸和硝酸钠处理含硒的工业废料,得到亚硒酸(H2SeO3)和少量硒酸(H2SeO4),富集后再将它们与盐酸共热,将H2SeO4转化为H2SeO3,主要反应为2HCl+H2SeO4 | |
| [ ] | |
A. |
H2SeO4的氧化性比Cl2弱 |
B. |
SeO2的氧化性比SO2弱 |
C. |
H2SeO4的氧化性比H2SeO3强 |
D. |
浓H2SeO4的氧化性比HNO3强 |
|
有一固体混合物,可能由Na2CO3、Na2SO4、CuSO4、CaCl2、NaCl混合而成,为检验它的成分,做了如下实验: ①将固体混合物溶于水,搅拌后得无色透明溶液; ②往此溶液中滴加硝酸钡溶液,有白色沉淀生成; ③过滤,将沉淀物置于稀硝酸中,发现沉淀全部溶解. 则该固体混合物中 | |
| [ ] | |
A. |
肯定有Na2SO4,可能有CuSO4 |
B. |
一定有NaCl,肯定没有Na2SO4 |
C. |
一定有Na2CO3,可能有NaCl |
D. |
可能有CaCl2,一定没有CuSO4 |
|
下列叙述正确的是 | |
| [ ] | |
A. |
氯水通入SO2后溶液的酸性减弱 |
B. |
向明矾溶液中加入过量NaOH溶液会产生大量白色沉淀 |
C. |
Na、Mg、Fe等金属在一定条件下与水反应都生成H2和对应的碱 |
D. |
浓硫酸、浓硝酸在加热条件下都能将木炭氧化为二氧化碳 |
|
关于SO2的叙述中,正确的是 | |
| [ ] | |
A. |
在有的反应中显示氧化性,有的反应中显示还原性 |
B. |
是酸性氧化物,溶于水得稳定的亚硫酸 |
C. |
SO2气体通入NaOH溶液中一定得到Na2SO3 |
D. |
SO2气体通入BaCl2溶液中,能生成白色沉淀 |
|
对某酸性溶液(可能含有Br-,SO ①加热时放出的气体可以使品红溶液褪色; ②加碱调至碱性后,加热时放出的气体可以使润湿的红色石蕊试纸变蓝; ③加入氯水时,溶液略显黄色,再加入BaCl2溶液,产生的白色沉淀不溶于稀硝酸. 对于下列物质不能确认其在原溶液中是否存在的是 | |
| [ ] | |
A. |
Br- |
B. |
SO |
C. |
H2SO3 |
D. |
NH |
|
同温同压下,在3支相同体积的试管中分别充有等体积混合的2种气体,它们是①NO和NO2,②NO2和O2,③NH3和N2.现将3支试管均倒置于水槽中,充分反应后,试管中剩余气体的体积分别为V1、V2、V3,则下列关系正确的是 | |
| [ ] | |
A. |
V1>V2>V3 |
B. |
V1>V3>V2 |
C. |
V2>V3>V1 |
D. |
V3>V1>V2 |
|
有9.7 g Cu和Zn的合金与足量的稀HNO3反应,还原产物只有NO气体,其体积在标准状况下为2.24 L.将溶液稀释为1 L,测得溶液的pH=1,此时溶液中NO | |
| [ ] | |
A. |
0.3 mol/L |
B. |
0.4 mol/L |
C. |
0.5 mol/L |
D. |
0.6 mol/L |