|
甲在常温时为离子晶体,由X、Y两种元素组成,在甲中Xm+和Yn–的电子结构相同,甲、乙、丙、丁、戊、己之间有如下反应关系: ①甲+H2O ②H2+丙→丁(气体) ③乙+丙→甲+戊+H2O ④戊+丁→甲+己(酸性) 甲、戊、己依次是 | |
| [ ] | |
A. |
NaCl、NaClO、HClO |
B. |
Na2S、Na2SO3、H2SO3 |
C. |
CaCl2、Ca(ClO)2、HClO |
D. |
K2S、K2SO3、H2SO4 |
|
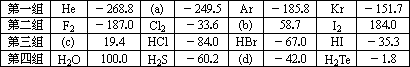
有四组同族元素的物质,在101.3 kPa时测定它们的沸点(℃)如下表所示:
下列各项中正确的是 | |
| [ ] | |
A. |
a、b、c的化学式分别为Ne2、Br2、HF |
B. |
第二组物质只表现氧化性,不表现还原性 |
C. |
第三组物质中C的沸点最高,是因为C分子内存在氢键 |
D. |
第四组中各化合物的稳定性顺序为:H2O>H2S>H2Se>H2Te |
|
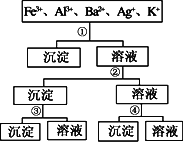
用过量的H2SO4、NaOH、NH3·H2O、NaCl等溶液,按如图所示步骤分开五种离子,则溶液①、②、③、④是
| |
| [ ] | |
A. |
①NaCl;②NaOH;③NH3·H2O;④H2SO4 |
B. |
①H2SO4;②NaOH;③NH3·H2O;④NaCl |
C. |
①H2SO4;②NH3·H2O;③NaOH;④NaCl |
D. |
①NaCl;②NH3·H2O;③NaOH;④H2SO4 |
|
下列反应的离子方程式正确的是 | |
| [ ] | |
A. |
将标准状况下112 mL氯气通入10 mL 1 mol/L的溴化亚铁溶液中: 2Fe2++4Br-+3Cl2 |
B. |
滴有稀硫酸的淀粉碘化钾溶液在空气中变蓝:2I-+O2+4H+ |
C. |
SO2溶液使酸性KMnO4溶液褪色:5SO2+2MnO |
D. |
向次氯酸钙溶液中通入SO2:Ca2++2ClO-+SO2+H2O |
|
将0.4 g NaOH和1.06 g Na2CO3混合并配成溶液,向溶液中滴加0.1 mol·L-1稀盐酸.下列图象能正确表示加入盐酸的体积和生成CO2的物质的量的关系的是 | |
| [ ] | |
A. |
|
B. |
|
C. |
|
D. |
|
|
向Fe2O3和铁粉组成的混合物中,加入适量的稀H2SO4,各物质恰好完全反应,测得溶液中不含Fe3+,且Fe2+与H2的物质的量之比为4∶1,那么在反应中,Fe2O3、Fe、H2SO4的物质的量之比为 | |
| [ ] | |
A. |
1∶1∶1 |
B. |
1∶2∶4 |
C. |
1∶2∶3 |
D. |
2∶3∶5 |
|
在恒温、恒容下,发生如下反应:2A(g)+2B(g) | |
| [ ] | |
A. |
达到平衡时,途径Ⅰ的反应速率等于途径Ⅱ的反应速率 |
B. |
达到平衡时,途径Ⅰ所得混合气体的压强等于途径Ⅱ所得混合气体的压强 |
C. |
两途径最终达到平衡时,体系内各组分的百分含量相同 |
D. |
两途径最终达到平衡时,体系内各组分的百分含量不相同 |
|
下列反应的离子方程式书写正确的是 | |
| [ ] | |
A. |
氯化铝溶液中加入过量氨水:Al3++4NH3·H2O |
B. |
澄清石灰水与少量苏打溶液混合:Ca2++OH-+HCO |
C. |
碳酸钙溶于醋酸:CaCO3+2H+ |
D. |
氯化亚铁溶液中通入氯气:2Fe2++Cl2 |
|
室温下,下列溶液中的离子一定能大量共存的是 | |
| [ ] | |
A. |
c(H+)=1×10-13 mol·L-1的溶液中:Na+、CH3COO-、SO42-、AlO2- |
B. |
0.1 mol·L-1 FeCl3溶液中:K+、Mg2+、SCN-、NO3- |
C. |
pH=1的溶液中:K+、Fe2+、Cl-、NO3- |
D. |
水电离的c(H+)=10-12 mol·L-1的溶液中:Mg2+、NH4+、HCO3-、Cl- |
|
用NA表示阿伏加德罗常数的值.下列说法正确的是 | |
| [ ] | |
A. |
46 g乙醇溶液中,含氧原子数为NA |
B. |
1 mol Na2O2晶体中,含阴离子数为2NA |
C. |
25℃时,1.0 L pH=7的NH4Cl和NH3·H2O混合溶液中,OH-离子数为10-7NA |
D. |
在KClO3+6HCl |