|
下列关系不正确的是 | |
| [ ] | |
A. |
离子半径:Cl->F->Na+>Al3+ |
B. |
熔点:石英>食盐>冰>干冰 |
C. |
结合氢离子的能力:SO42->SO32->CO32- |
D. |
热稳定性:HF>HCl>H2S>PH3 |
|
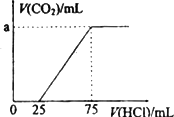
取一定量的NaOH溶液通入CO2后,再继续向该溶液中逐滴加入0.1 mol/L的盐酸,标准状况下产生的CO2的体积与所加盐酸体积之间的关系如下图所示,下列有关说法正确的是
| |
| [ ] | |
A. |
原溶液中NaOH的物质的量为0.75 mol |
B. |
通入CO2后所得的溶液溶质成分为NaOH和Na2CO3 |
C. |
通入CO2后所得的溶液中含有2.5×10-3 mol NaHCO3 |
D. |
纵坐标中a的数值为224 |
|
混合下列各组物质使之充分反应,加热蒸干产物并在300℃灼烧至质量不变,最终残留固体不是纯净物的是 | |
| [ ] | |
A. |
向Fe、FeO和Fe2O3的混合物中加入过量的盐酸 |
B. |
等物质的量浓度、等体积的(NH4)2SO4与BaC12溶液 |
C. |
等物质的量的NaHCO3溶液与Na2O2固体 |
D. |
在NaBr溶液中通入过量氯气 |
|
下列反应的离子方程式正确的是 | |
| [ ] | |
A. |
氢氧化铁溶于氢碘酸中:Fe(OH)3+3H+=Fe3++3H2O |
B. |
碳酸钠溶液显碱性:CO32-+2H2O |
C. |
NO2与水的反应:3NO2+H2O=2NO3-+NO↑+2H+ |
D. |
向次氯酸钙溶液通入SO2:Ca2++2ClO-+H2O+SO2=CaSO3↓+2HClO |
|
设NA为阿伏加德罗常数的值,下列叙述错误的是 | |
| [ ] | |
A. |
1 L 0.1 mol/L的NH4NO3溶液中氮原子数为0.2NA |
B. |
11.2 L O2和CO2的混合气体中含有氧原子的个数为NA |
C. |
7.8 g过氧化钠与CO2充分反应,转移的电数为0.1NA |
D. |
25℃时,pH=12的1.0 L NaClO溶液中水电离出的OH-的数目为0.01NA |
|
某无色溶液可能存在Al3+、H+、Na+、SO | |
| [ ] | |
A. |
一定存在的离子是Na+、SO |
B. |
一定存在的离子是Na+、SO |
C. |
可能存在的离子是Al3+、CO |
D. |
可能存在的离子是CO |
|
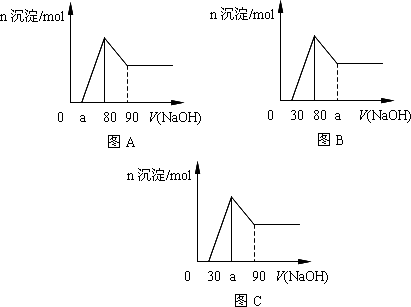
把一块镁铝合金投入到1 mol/L盐酸里,待合金完全溶解后,往溶液里加入1 mol/L NaOH溶液,生成沉淀的物质的量随加入NaOH溶液体积变化的关系如下图A所示.下列说法中不正确的是
| |
| [ ] | |
A. |
a的取值范围为0≤a<50 |
B. |
|
C. |
若将关系图改为B图时,则a的取值范围为80<a<90 |
D. |
若将关系图改为C图时,则a的取值范围为75<a<90 |
|
向绝热恒容密闭容器中通入SO2和NO2,一定条件下使反应SO2(g)+NO2(g)
由图可得出的正确结论是 | |
| [ ] | |
A. |
反应在c点达到平衡状态 |
B. |
反应物浓度:a点小于b点 |
C. |
反应物的总能量低于生成物的总能量 |
D. |
Δt1=Δt2时,SO2的转化率:a-b段小于b-c段 |
|
一定条件下,将一定量的PCl5(g)通人密闭容器中,发生PCl5(g) | |
| [ ] | |
A. |
PCl3在平衡混合物中的体积分数约为33.3%[已知:M(PCl5)=208.5M(PCl3)=137.5] |
B. |
PCl5的转化率约为50% |
C. |
恒温恒容下往容器中再充入一定量的PCl5(g),再达到新平衡时,PCl3(g)的体积分数比原平衡时大 |
D. |
恒温恒压下往容器中再充人一定量的PCl5(g),再达到新平衡时,c(PCl5)∶c(PCl3)∶c(Cl2)约为1∶1∶1 |
|
下列物质的检验,其结论一定正确的是 | |
| [ ] | |
A. |
某溶液中加入BaCl2溶液,产生白色沉淀,加入HNO3后,沉淀不溶解,则该溶液中一定含有SO42- |
B. |
某溶液中加入盐酸能产生使澄清石灰水变浑浊的气体,则该溶液中至少有SO32-和CO32-中的一种 |
C. |
取少量Na2SO3样品于试管中加水溶解后加入盐酸有气体产生,再加入BaCl2溶液有白色沉淀产生,说明Na2SO3样品已部分被氧化 |
D. |
能使湿润的碘化钾淀粉试纸变蓝的一定是Cl2 |