|
已知某化学反应的平衡常数表达式为K=
下列有关叙述不正确的是 | |
| [ ] | |
A. |
该反应的化学方程式是:CO(g)+H2O(g) |
B. |
上述反应的正反应是放热反应 |
C. |
如果在一定体积的密闭容器中加入CO2和H2各1 mol,5 min后温度升高到830℃,此时测得CO为0.4 mol时,该反应为平衡状态 |
D. |
某温度下,如果平衡浓度符合下列关系式: |
|
下 列各溶液中,物质的量浓度关系正确的是 | |
| [ ] | |
A. |
在0.1 mol·L-1 CH3COONa溶液中,c(OH-)=c(CH3COOH)+c(H+) |
B. |
常温下, 10 mL 0.01 mol·L-1HCl溶液与10 mL 0.01 mol·L-1 Ba(OH)2溶液充分混合,若混合后溶液的体积为20 mL,则溶液的pH=12 |
C. |
0.1 mol·L-1的KAl(SO4)2溶液中:c(SO42-)>c(Al3+)>c(OH-)>c(H+) |
D. |
等体积、等物质的量浓度的NaX和弱酸HX混合后的溶液,若溶液呈酸性,则有c(Na+)>c(HX)>c(X-)>c(H+)>c(OH-) |
|
下 图是一种航天器能量储存系统原理示意图.下列说法正确的是
| |
| [ ] | |
A. |
该系统中只存在3种形式的能量转化 |
B. |
装置X能实现燃料电池的燃料和氧化剂再生 |
C. |
装置Y中负极的电极反应式为:O2+2H2O+4e-=4OH- |
D. |
装置X、Y形成的子系统能实现物质的零排放,并能实现化学能与电能间的完全转化 |
|
已知可逆反应X(g)+Y(g)
| |
| [ ] | |
A. |
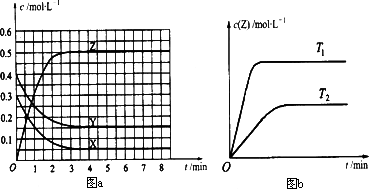
发生反应时,各物质的反应速率大小关系为:v(X)=v(Y)=2v(Z) |
B. |
图a中反应达到平衡时,Y的转化率为37.5% |
C. |
T0℃时,该反应的平衡常数为33.3 |
D. |
该反应正反应的反应热ΔH<0 |
|
J、M、R、T是原子序数依次增大的短周期主族元素,J、R在周期表中的相对位置如下表.已知J元素最低负化合价的绝对值与其原子最外层电子数相等,M是地壳中含量最多的金属元素.下列说法错误的是
| |
| [ ] | |
A. |
J和氢组成的化合物分子中只含有极性共价键 |
B. |
工业上用电解熔融的M的氧化物方法来制备M |
C. |
R、T两元素的气态氢化物中,T的气态氢化物更稳定 |
D. |
J、M、R、T元素最高价氧化物对应的水化物中酸性最强的是HTO4 |
|
下列离子反应方程式正确的是 | |
| [ ] | |
A. |
用 澄清石灰水来吸收氯气:Cl2+OH-=Cl-+ClO-+H+ |
B. |
向稀硝酸中加入少量铁粉:3Fe+8H++2NO3-=3Fe2++2NO↑+4H2O |
C. |
将金属钠加入冷水中:2Na+2H2O=2Na++2OH-+H2↑ |
D. |
碳酸氢钙溶液中加入少量苛性钾溶液:Ca2++2HCO3-+2OH-=CaCO3↓+CO32-+2H2O |
|
设NA是阿伏加德罗常数的数值,下列说法不正确的是 | |
| [ ] | |
A. |
常温下,23 g NO2含有NA个氧原子 |
B. |
1 mol Cl2与足量的铁反应,转移的电子数为3NA |
C. |
0.1 mol 24Mg32S晶体中所含中子总数为2.8 NA |
D. |
用惰性电极电解硫酸铜溶液,若生成1 mol O2,则转移电子数为4NA |
|
室温下, 下列各组离子在给定条件下一定能大量共存的是 | |
| [ ] | |
A. |
含有大量NO3-的水溶液中:NH4+、Fe2+、SO42-、H+ |
B. |
在pH=12的溶液中:ClO-、SO32-、Na+、K+ |
C. |
c(H+)=1.0×10-13 mol/L溶液中:C6H5O- 、K+、SO42-、Br- |
D. |
能与铝粉反应生成氢气的溶液中:Na+、Al3+、CH3COOO-、I- |
|
氮化钠和氢化钠都是离子化合物,与水反应的化学方程式(未配平)如下:Na3N+H2O→NaOH+NH3,NaH+H2O→NaOH+H2.有关它们的叙述 ① 离子半径Na+>N3->H+;②与水反应都是氧化还原反应; ③与水反应后的溶液都显碱性; ④与盐酸反应都只生成一种盐; ⑤两种化合物中的阴阳离子均具有相同的电子层结构. 其中正确的是 | |
| [ ] | |
A. |
②③④⑤ |
B. |
①③⑤ |
C. |
②④ |
D. |
③ |
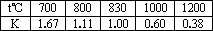
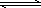 CO2(g)+H2(g)
CO2(g)+H2(g)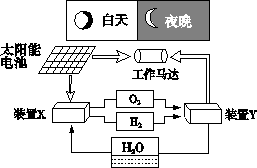
 Z(g)(未配平).温度为T0时,在容积固定的容器中发生反应各物质的浓度随时间变化的关系如图a所示.其他条件相同,温度分别为T1、T2时发生反应,Z的浓度随时间变化的关系如图b所示.下列叙述正确的是
Z(g)(未配平).温度为T0时,在容积固定的容器中发生反应各物质的浓度随时间变化的关系如图a所示.其他条件相同,温度分别为T1、T2时发生反应,Z的浓度随时间变化的关系如图b所示.下列叙述正确的是