|
下列各组在溶液中的反应,不管反应物量的多少,都只能用同一个离子方程式来表示的是 | |
| [ ] | |
A. |
FeBr2和Cl2 |
B. |
Ba(OH)2与H2SO4 |
C. |
HCl与Na2CO3 |
D. |
Ca(HCO3)2与NaOH |
|
用NA表示阿伏加德罗常数的值.下列叙述正确的是 | |
| [ ] | |
A. |
标准状况下,22.4 L己烷中共价键数目为19NA |
B. |
0.1 mol Fe与足量硫粉充分反应,转移的电子数为0.3NA |
C. |
1 mol/L的Na2CO3溶液中含有NA个CO |
D. |
由CO2和O2组成的混合物中共有NA个分子,其中的氧原子数为2NA |
|
下列离子方程式正确的是 | |
| [ ] | |
A. |
硫化钠的水解反应:S2-+H3O+ |
B. |
氧化铝溶解在NaOH溶液中:3H2O+Al2O3+2OH- |
C. |
明矾溶液与氢氧化钡溶液反应 ,使SO42-恰好沉淀完全Al3++SO42-+Ba2++4OH-=BaSO4↓+AlO2-+2H2O |
D. |
用惰性电极电解饱和氯化镁溶液 :2Cl-+2H2O 2OH-+H2↑+Cl2↑ 2OH-+H2↑+Cl2↑
|
|
某溶液加入铝能产生氢气.则下列各组离子,在该水溶液中可以大量共存的是 | |
| [ ] | |
A. |
Fe2+、K+、Cl-、NO |
B. |
K+、Mg2+、Cl-、SO |
C. |
Na+、Fe3+、CO |
D. |
NH |
|
设nA为阿伏加德罗常数的数值,下列说法正确的是 | |
| [ ] | |
A. |
16 g CH4中含有4nA个C-H键 |
B. |
1 mol/L NaCl溶液含有nA个Na+ |
C. |
1 mol Cu和足量稀硝酸反应产生nA个NO分子 |
D. |
标准状况下,22.4 L己烯中含有nA个CO2分子 |
|
设NA代表阿伏加德罗常数的数值,下列说法中正确的是 ①常温常压下,17 g甲基(-14CH3)所含的中子数为9NA ②常温常压下,22.4 L NO气体的分子数小于NA ③64 g铜发生氧化还原反应,一定失去2NA个电子 ④常温常压下,100 mL 0.5 mol/L的乙酸溶液中,乙酸的分子数目小于0.05NA ⑤标准状况下,22.4 L二氯甲烷所含有的分子数为NA ⑥常温常压下,1 mol氦气含有的核外电子数为4NA | |
| [ ] | |
A. |
①② |
B. |
③④ |
C. |
②④ |
D. |
⑤⑥ |
|
镍镉(Ni-Cd)可充电电池在现代生活中有广泛应用.已知某镍镉电池的电解质溶液为氢氧化钾溶液,其充放电按下式进行:Cd+2NiO(OH)+H2O | |
| [ ] | |
A. |
充电时阳极反应:Ni(OH)2+OH- |
B. |
充电过程是化学能转化为电能的过程 |
C. |
放电时负极附近的溶液的碱性不变 |
D. |
放电时电解质溶液中的OH-向正极移动 |
|
可以证明可逆反应N2+3H2 ①一个NN叁键断裂的同时,有3个H-H键断裂; ②一个NN叁键断裂的同时,有6个N-H键断裂; ③其他条件不变时,混合气体平均相对分子质量不再改变; ④保持其他条件不变时,体系压强不再改变; ⑤NH3%、N2%、H2%都不再改变; ⑥恒温、恒容时,密度保持不变; ⑦正反应速率v(H2)=0.6 mol·(L·min)-1,逆反应速率v(NH3)=0.4 mol·(L·min)-1. | |
| [ ] | |
A. |
全部 |
B. |
①③④⑤ |
C. |
②③④⑤⑦ |
D. |
①③⑤⑥⑦ |
|
在373 K时,把0.5 mol N2O4气通入体积为5 L的真空密闭容器中立即出现红棕色,反应进行到2 s时,NO2的浓度为0.02 mol/L,在60 s时体系达到平衡,此时容器内压强为开始压强的1.6倍.下列说法正确的是 | |
| [ ] | |
A. |
前2 s v( N2O4) =0.01 mol/( L·s) |
B. |
2 s时体系内压强为开始时的1.1倍 |
C. |
平衡时体系内含N2O4 0.25 mol |
D. |
平衡时若压缩容器体积可提高N2O4的转化率 |
|
下列混合溶液中,各离子浓度的大小顺序正确的是 | |
| [ ] | |
A. |
10 mL 0.1 mol·L-1氨水与10 mL 0.1 mol·L-1盐酸混合,c(Cl-)>c(NH |
B. |
10 mL 0.1 mol·L-1 NH4Cl溶液与5 mL 0.2 mol·L-1 NaOH溶液混合,c(Na+)=c(Cl-)>c(OH-)>c(H+) |
C. |
10 mL 0.1 mol·L-1 CH3COOH溶液与10 mL 0.2 mol·L-1 NaOH溶液混合,c(Na+)=c(CH3COO-)>c(OH-)>c(H+) |
D. |
10 mL 0.5 mol·L-1 CH3COONa溶液与5 mL 1 mol·L-1盐酸混合,c(Cl-)>c(Na+)>c(OH-)>c(H+) |
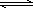 HS-+H2O
HS-+H2O 2Al(OH)4-
2Al(OH)4-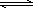 Cd(OH)2+2Ni(OH)2.下列有关电池的说法正确的是:
Cd(OH)2+2Ni(OH)2.下列有关电池的说法正确的是: NiO(OH)+H2O+e-
NiO(OH)+H2O+e-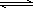 2NH3已达到平衡状态的是
2NH3已达到平衡状态的是