|
下列离子在指定溶液中一定能大量共存的是 ①加入Al能放出H2的溶液中:Fe2+、Al3+、NO ②在pH=11的溶液中:Na+、AlO ③由水电离的c(H+)=10-12 mol·L-1的溶液中:Cl-、HCO ④加入Mg能放出H2的溶液中:Mg2+、NH | |
| [ ] | |
A. |
②④ |
B. |
①②④ |
C. |
①③④ |
D. |
①② |
|
下列离子方程式中,只能表示一个化学反应的是 ①Fe+Cu2+ ②Ba2++2OH-+2H++SO ③Cl2+H2O ④CO ⑤Ag++Cl- | |
| [ ] | |
A. |
只有 ③ |
B. |
②③ |
C. |
③⑤ |
D. |
①④ |
|
设NA为阿伏加德罗常数的值,下列叙述中错误的是 | |
| [ ] | |
A. |
在标准状况下,22.4 L空气中约有NA个气体分子 |
B. |
在含4 mol Si-O键的石英晶体中,氧原子的数目为2NA |
C. |
28 g乙烯和28 g丙烯中均含有6NA对共用电子对 |
D. |
含NA个氧原子的O2与含NA个氧原子的O3的质量之比为2∶3 |
|
碘是一种与人的生命活动密切相关的元素 ,已知碘单质能溶于NaOH或KI溶液,反应方程式分别为:I2+6OH- 5I-+IO3-+3H2O(HIO不稳定,易发生歧化反应)和I2+I-=I3-,溴化碘(IBr)是一种卤素互化物,具有与卤素单质类似的性质,下列反应方程式正确的有 5I-+IO3-+3H2O(HIO不稳定,易发生歧化反应)和I2+I-=I3-,溴化碘(IBr)是一种卤素互化物,具有与卤素单质类似的性质,下列反应方程式正确的有
| |
| [ ] | |
A. |
IBr 加入Na2S溶液中产生淡黄色浑浊:2IBr+S2- 2I-+2Br-+S↓ 2I-+2Br-+S↓
|
B. |
少量 IBr加入KI溶液中:IBr+I-=Br-+I2 |
C. |
IBr 加入NaOH溶液中:IBr+2OH- I-+BrO-+H2O I-+BrO-+H2O
|
D. |
IBr 加入AgNO3溶液中:3IBr+5Ag++3H2O 3AgBr↓+2AgI↓+IO3-+6H+ 3AgBr↓+2AgI↓+IO3-+6H+
|
|
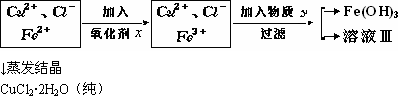
氯化铜(CuCl2·2H2O)中含FeCl2杂质.为制得纯净氯化铜晶体,首先将其制成水溶液,然后按下面所示操作步骤进行提纯.
氧化剂x与物质Y的化学式分别是(已知完全成氢氧化物所需pH值:Fe3+为3.7,Cu2+为6.4,Fe2+为9.6.) | |
| [ ] | |
A. |
H2O2、CuO |
B. |
KMnO4、Na2O |
C. |
NaClO、Cu(OH)2 |
D. |
K2Cr2O7、NaOH |
|
在由Fe、FeO和Fe2O3组成的混合物中加入100 mL 2 mol/L的盐酸,恰好使混合物完全溶解,并放出448 mL气体(标准状况),此时溶液中无Fe3+离子.则下列判断正确的是 | |
| [ ] | |
A. |
混合物里三种物质反应时消耗盐酸的物质的量之比为1∶1∶3 |
B. |
反应后所得溶液中的Fe2+离子与Cl- 离子的物质的量之比为2∶1 |
C. |
混合物里,FeO的物质的量无法确定,但Fe比Fe2O3的物质的量多 |
D. |
混合物里,Fe2O3的物质的量无法确定,但Fe比FeO的物质的量多 |
|
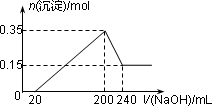
将一定质量的镁和铝混合物投入200 mL硫酸中,固体全部溶解后,向所得溶液中加入NaOH溶液,生成沉淀的物质的量n与加入NaOH溶液的体积V的变化如图所示.则下列说法不正确的是
| |
| [ ] | |
A. |
镁和铝的总质量为9 g |
B. |
最初20 mL NaOH溶液用于中和过量的硫酸 |
C. |
硫酸的物质的量浓度为2.5 mol·L-1 |
D. |
生成的氢气在标准状况下的体积为11.2 L |
|
实验室将I2溶于KI溶液中,配制浓度较大的碘水,主要是因为发生了反应: I2(aq)+I-(aq)
| |
| [ ] | |
A. |
该反应的正反应是吸热反应 |
B. |
A点与C点的化学反应速度vA<vC |
C. |
在反应进行到D点时,v(正)>v(逆) |
D. |
A点与B点相比,B点的c(I2)大 |
|
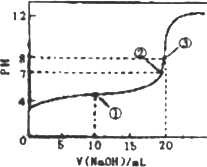
常温下,用0.1000 mol·L-1 NaOH溶液滴定20.00 mL 0.1000 mol·L-1 CH3COOH溶液,滴定曲线如下图.下列说法正确的是
| |
| [ ] | |
A. |
点①所示溶液中:[CH3COO-]+[OH-]=[CH3COOH]+[H+] |
B. |
点②所示溶液中:[Na+]=[CH3COOH]+[CH3COO-] |
C. |
点③所示溶液中:[Na+]>[OH-]>[CH3COO-]>[H+] |
D. |
滴定过程中可能出现:[CH3COOH]>[CH3COO-]>[H+]>[Na+]>[OH-] |
|
下列对各种平衡体系的叙述中,完全正确的是一组是 ①在醋酸溶液中存在的电离平衡:CH3COOH ②常温下,在醋酸溶液中加入少量的CH3COONa固体,会使其电离平衡逆向移动; ③某温度下,容积一定的密闭容器中进行可逆反应:X(g)+Y(g) ④在上述③的可逆反应中,当容器中气体压强不变时,反应达到平衡; ⑤一定浓度的醋酸钠溶液可使酚酞试液变红,其原因是溶液中存在如下平衡: CH3COO-+H2O ⑥在碳酸钙的沉淀溶解平衡体系中,加入稀盐酸,平衡向溶解的方向移动 ⑦在氯化银的沉淀溶解平衡体系中,加入碘化钾固体,氯化银沉淀可转化为碘化银沉淀 | |
| [ ] | |
A. |
①②③④⑤ |
B. |
②③④⑤⑥ |
C. |
②③⑤⑥⑦ |
D. |
①②⑤⑥⑦ |
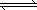 I3-(aq),上述平衡体系中,I3-的物质的量浓度c(I3-)与温度T的关系如图所示(曲线上的任何一点都表示平衡状态).下列说法不正确的是
I3-(aq),上述平衡体系中,I3-的物质的量浓度c(I3-)与温度T的关系如图所示(曲线上的任何一点都表示平衡状态).下列说法不正确的是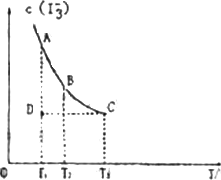
 CH3COO-+H+,加水稀释后,溶液中所有离子浓度均减小;
CH3COO-+H+,加水稀释后,溶液中所有离子浓度均减小; 2Z(g)+W(s);ΔH>0平衡后,升高温度,该化学平衡正向移动;
2Z(g)+W(s);ΔH>0平衡后,升高温度,该化学平衡正向移动; CH3COOH+OH-
CH3COOH+OH-