|
今有一混合物的水溶液,只可能含有以下离子中的若干种:K+、 (1)第一份加入AgNO3溶液有沉淀产生 (2)第二份加足量NaOH溶液加热后,收集到气体0.04 mol (3)第三份加足量BaCl2溶液后,得干燥沉淀6.27 g,经足量盐酸洗涤、干燥后,沉淀质量为2.33 g.根据上述实验,以下推测正确的是 | |
| [ ] | |
A. |
K+一定存在 |
B. |
100 mL溶液中含0.01 mol CO |
C. |
Cl-一定存在 |
D. |
Ba2+一定不存在,Mg2+可能存在 |
|
下列说法中正确的是 | |
| [ ] | |
A. |
在相同条件下,若将等量的硫蒸气和硫固体分别完全燃烧,后者放出热量多 |
B. |
由“C(石墨)=C(金刚石)ΔH=+1.9 kJ·mol-1”可知,金刚石比石墨稳定 |
C. |
在稀溶液中:H+(aq)+OH-(aq)=H2O(1);ΔH=-57.31 kJ·mol-1,若将含0.5 mol H2SO4的浓硫酸与1 mol NaOH溶液混合,放出的热量大于57.31 kJ |
D. |
在101 Kpa时,2 g H2完全燃烧生成液态水,放出285.8 kJ热量,氢气燃烧的热化学方程式表示为:2H2(g)+O2(g)=2H2O(1);ΔH=+258.8 kJ·mol-1 |
|
下列离子方程式书写正确的是 | |
| [ ] | |
A. |
过量的SO2通入NaOH溶液中:SO2+2OH-=SO |
B. |
Fe(NO3)3溶液中加入过量的HI溶液:2Fe3++2I-=2Fe2++I2 |
C. |
NaNO2溶液中加入酸性KMnO4溶液:2MnO |
D. |
NaHCO3溶液中加入过量的Ba(OH)2溶液:2HCO |
|
下列说法不正确的是 | |
| [ ] | |
A. |
1 mol氧气中含有12.04×1023个氧原子,在标准状况下占有体积约为22.4 L |
B. |
等体积、浓度均为1 mol/L的磷酸和盐酸,电离出的氢离子数之比为3∶1 |
C. |
1 mol臭氧和1.5 mol氧气含有相同的氧原子数 |
D. |
等物质的量的干冰和葡萄糖中所含碳原子数之比为1∶6,氧原子数之比为1∶3 |
|
下列各组离子在给定条件下能大量共存的是 | |
| [ ] | |
A. |
在pH=1溶液中: |
B. |
有 |
C. |
有 |
D. |
在 |
|
下列离子方程式书写正确的是 | |
| [ ] | |
A. |
溴乙烷与6 mol/L的氢氧化钠水溶液共热:C2H5Br+OH- |
B. |
等物质的量浓度、等体积的Ca(HCO3)2溶液与氢氧化钠溶液相混合:Ca2++2HCO3-+2OH- |
C. |
在含有等物质的量的Fe(NO3)2和KI组成的混合溶液中滴入1~2滴盐酸:3Fe2++4H++NO3- |
D. |
在 H2O2中加入酸性高锰酸钾溶液:2MnO4-+6H++5H2O2 |
|
在下列给定条件的溶液中,一定能大量共存的离子组是 | |
| [ ] | |
A. |
无色溶液:Ca2+、H+、Cl-、HSO3- |
B. |
能使pH试纸呈红色的溶液:Na+、NH4+、I-、NO3- |
C. |
FeCl2溶液:K+、Na+、SO42-、AlO2- |
D. |
|
|
下列离子方程式与所述事实相符且正确的是 | |
| [ ] | |
A. |
漂白粉溶液在空气中失效:ClO-+CO2+H2O |
B. |
用浓盐酸与MnO2反应制取少量氯气:MnO2+2H++2Cl- |
C. |
向 NaAlO2溶液中通入过量CO2制Al(OH)3:AlO2-+CO2+2H2O |
D. |
在强碱溶液中次氯酸钠与 Fe(OH)3反应生成Na2FeO4:3ClO-+2Fe(OH)3 |
|
向10.00 ml 0.01 mol/L某一元酸HA溶液 中逐滴加入0.01 mol/L NaOH溶液,溶液pH变化曲线如图所示.下列说法不正确的是
| |
| [ ] | |
A. |
HA是弱酸 |
B. |
b点表示的溶液中:2c(Na+)=c(A-)+c(HA) |
C. |
b、c、d点表示的溶液中:c(Na+)+c(H+)=c(A-)+c(OH-) |
D. |
c点时:V=10.00 ml |
|
铁镍蓄电池又称爱迪生电池,放电时的总反应为:Fe+Ni2O3+3H2O 下列有关该电池的说法不正确的是 | |
| [ ] | |
A. |
电池的电解液为碱性溶液,正极为Ni2O3、负极为Fe |
B. |
电池放电时,负极反应为Fe+2OH--2e-=Fe(OH)2 |
C. |
电池充电过程中,阴极附近溶液的pH降低 |
D. |
电池充电时,阳极反应为2Ni(OH)2+2OH--2e-=Ni2O3+3H2O |
 Mn2++Cl2↑+2H2O
Mn2++Cl2↑+2H2O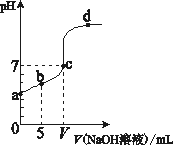
 Fe(OH)2+2Ni(OH)2
Fe(OH)2+2Ni(OH)2