|
常温下,下列各组离子在制定溶液中一定能大量共存的是 | |
| [ ] | |
A. |
1.0 mol·L-1的KNO3溶液:H+、Fe2+、Cl-、SO42- |
B. |
甲基橙呈红色的溶液:NH4+、Ba2+、AlO2-、Cl- |
C. |
pH=12的溶液:K+、Na+、CH3COO-、Br- |
D. |
与铝反应产生大量氢气的溶液:Na+、K+、CO32-、NO3- |
|
有人设计将两根Pt丝作电极插入KOH溶液中,然后向两极上分别通入甲烷和氧气而构成燃料电池.该电池中反应的化学方程式:CH4+2O2+2KOH | |
| [ ] | |
A. |
通入甲烷的电极为电池的正极,通入氧气的电极为负极 |
B. |
在标准状况下,每消耗5.6 L O2,可向外提供8.3×104 C的电量 |
C. |
通入甲烷电极的电极反应为:CH4+10OH――8e- |
D. |
放电一段时间后,溶液pH升高 |
|
金属镍有广泛应用.粗镍中含有少量Fe、Zn、Cu、Pt等杂质,可用电解法制备高纯度的镍,下列叙述正确的是(已知氧化性Fe2+<Ni2+<Cu2+) | |
| [ ] | |
A. |
阳极发生还原反应,其主要电极反应式:Ni2++2e- |
B. |
电解过程中,阳极质量的减少与阴极质量的增加相等 |
C. |
电解后,溶液中存在的金属阳离子只有Fe2+和Zn2+ |
D. |
电解后,电解槽底部的阳极泥中含有Cu和Pt |
|
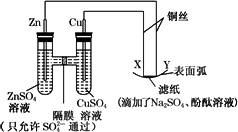
按下图所示装置做实验,若x轴表示流入阴极的电子的物质的量,则y轴可表示
①c(Ag+) ②c(NO ③a棒的质量 ④b棒的质量 ⑤溶液的pH | |
| [ ] | |
A. |
①③ |
B. |
③④ |
C. |
①②④ |
D. |
①②⑤ |
|
某溶液中含有两种溶质NaCl与H2SO4,它们的物质的量之比为3∶1.用石墨作电极电解该混合溶液时,根据电极产物,可明显分为三个阶段.下列叙述不正确的是 | |
| [ ] | |
A. |
阴极自始至终只有H2 |
B. |
阳极先析出Cl2后析出O2 |
C. |
电解最后阶段为电解水 |
D. |
溶液pH不断增大,最后为7 |
|
市场上经常见到的标记为Li-ion的电池称为“锂离子电池”.它的负极材料是金属锂和碳的复合材料(碳作为金属锂的载体),电解质为一种能传导Li+的高分子材料.这里锂离子电池的电池反应式为: Li+2Li0.35NiO2 | |
| [ ] | |
A. |
放电时,负极的电极反应式:Li-e- |
B. |
充电时,Li0.85NiO2既发生氧化反应又发生还原反应 |
C. |
该电池不能用水溶液作为电解质 |
D. |
放电过程中Li+向负极移动 |
|
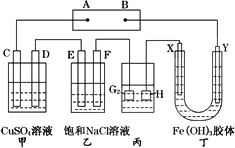
如图所示的装置,C、D、E、F、X、Y都是惰性电极.将电源接通后,向(乙)中滴入酚酞溶液,在F极附近显红色.则以下说法正确的是
| |
| [ ] | |
A. |
电源B极是正极 |
B. |
甲、乙装置的C、D、E、F电极均有单质生成,其物质的量之比为1∶2∶2∶2 |
C. |
欲用丙装置给铜镀银,H应该是Ag,电镀液是AgNO3溶液 |
D. |
装置丁中Y极附近红褐色变深,说明氢氧化铁胶粒带负电荷 |
|
下列浓度关系正确的是 | |
| [ ] | |
A. |
氯水中:c(Cl2)=2[c(ClO-)+c(Cl-)+c(HClO)] |
B. |
氯水中:c(Cl-)>c(H+)>c(OH-)>c(ClO-) |
C. |
等体积等浓度的氢氧化钠与醋酸混合:c(Na+)=c(CH3COO-) |
D. |
Na2CO3溶液中:c(Na+)>c(CO |
 K2CO3+3H2O,则关于此燃料电池的下列说法正确的是(一个电子所带电量为1.6×10-19 C)
K2CO3+3H2O,则关于此燃料电池的下列说法正确的是(一个电子所带电量为1.6×10-19 C) CO
CO
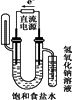

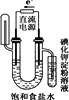
 Ni
Ni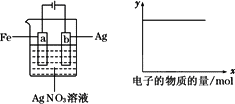
 Li+
Li+