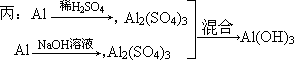|
关于第ⅥA族和第ⅦA族元素的下列说法中正确的是 | |
| [ ] | |
A. |
在同一周期,第ⅥA族元素氢化物的稳定性比第ⅦA族的强 |
B. |
浓度都是0.01 mol·L-1时,硫酸溶液的pH比高氯酸溶液的小 |
C. |
第ⅦA族单质的氧化性均比第ⅥA族单质的氧化性强 |
D. |
加热时,硫酸钠比氯酸钠易分解 |
|
已知BrCl能发生下列反应:nBrCl+2M=MCln+MBrn(M为+n价的金属元素),BrCl+H2O=HCl+HBrO,以下推论不正确的是 | |
| [ ] | |
A. |
BrCl具有和卤素单质相似的化学性质 |
B. |
BrCl和M反应时,BrCl只作氧化剂 |
C. |
BrCl和NaOH溶液反应生成NaCI、NaBrO两种盐 |
D. |
将BrCl跟FeSO4溶液反应,溶液会变成无色 |
|
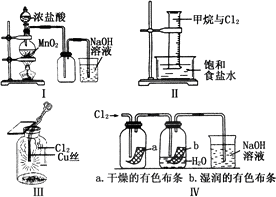
某同学用下列装置制备并检验Cl2的性质. 下列说法正确的是
| |
| [ ] | |
A. |
Ⅰ图中:如果MnO2过量,浓盐酸就可全部消耗 |
B. |
Ⅱ图中:量筒中发生了加成反应 |
C. |
Ⅲ图中:生成蓝色的烟 |
D. |
Ⅳ图中:湿润的有色布条能褪色,将硫酸溶液滴入烧杯中,至溶液显酸性,结果有Cl2生成 |
|
标准状况下,将a L H2和Cl2的混合气体点燃,充分反应后,将混合气体通入含b mol NaOH的热溶液中,气体恰好被完全吸收,NaOH无剩余,测得反应后溶液中含Cl-、ClO-、ClO | |
| [ ] | |
A. |
a/2 mol |
B. |
(a/22.4-b)mol |
C. |
(a/22.4-b/2)mol |
D. |
b/2mol |
|
下列离子方程式正确的是 ①氯气与水反应:Cl2+H2O ②氯气与氢氧化钠溶液反应:Cl2+2OH- ③浓盐酸与二氧化锰共热:MnO2+4HCl ④漂白粉溶液中通入少量的二氧化碳气体:Ca2++2ClO-+H2O+CO2 | |
| [ ] | |
A. |
①③ |
B. |
②④ |
C. |
②③ |
D. |
①④ |
|
向m g镁和铝的混合物中加入适量的稀硫酸,恰好完全反应生成标准状况下的气体b L.向反应后的溶液中加入c mol/L氢氧化钾溶液V mL,使金属离子刚好沉淀完全,得到的沉淀质量为n g.再将得到的沉淀灼烧至质量不再改变为止,得到固体p g.则下列关系不正确的是 | |
| [ ] | |
A. |
c= |
B. |
p=m+ |
C. |
n=m+17 Vc |
D. |
|
|
下列各反应的离子方程式中,错误的是 | |
| [ ] | |
A. |
硫酸铝溶液中加入过量的氨水: Al3++3NH3·H2O |
B. |
铁片放入过量的稀硝酸中: 3Fe+8H++2NO |
C. |
将铝片放入过量NaOH溶液中: 2Al+2OH-+2H2O |
D. |
偏铝酸钠与过量盐酸反应: AlO |
|
用稀硫酸、NaOH溶液、Al为原料制取Al(OH)3,甲、乙、丙3个学生分别用3种不同途径: 甲 :Al乙 :Al
制得等量 Al(OH)3,下列结论正确的是 | |
| [ ] | |
A. |
甲用原料最少 |
B. |
乙用原料最少 |
C. |
丙用原料最少 |
D. |
三人用原料的量相同 |
|
200℃时,11.6 g CO2和水蒸气的混合气体与过量的Na2O2充分反应后,固体质量增加了3.6 g,再将反应后剩余固体冷却后加入含有Na+、HCO | |
| [ ] | |
A. |
原混合气体的平均摩尔质量为23.2 g/mol |
B. |
混合气体与Na2O2反应过程中电子转移的物质的量为0.25 mol |
C. |
溶液中SO |
D. |
溶液中HCO |
|
取一支大试管,加入20 mL饱和澄清石灰水(ρ=1.6 g·cm-3),再加入5 mL苯(ρ=0.87 g·cm-3),静置后缓慢加入黄豆粒大小的钠块(ρ=0.97 g·cm-3).下列实验现象中,能观察到的有 ①钠在饱和澄清石灰水层反应并四处游动 ②有气体产生 ③澄清石灰水变浑浊 ④钠在石灰水与苯的界面处反应并上下跳动 ⑤钠停留在苯层不反应 ⑥钠块最后消失 | |
| [ ] | |
A. |
①②⑥ |
B. |
②③④⑥ |
C. |
⑤ |
D. |
①②③⑥ |
 2H++Cl-+ClO-
2H++Cl-+ClO- Cl-+ClO-+H2O
Cl-+ClO-+H2O Mn2++2Cl-+Cl2↑+2H2O
Mn2++2Cl-+Cl2↑+2H2O CaCO3↓+2HClO
CaCO3↓+2HClO Al(OH)3↓+3NH
Al(OH)3↓+3NH 3Fe2++2NO2↑+4H2O
3Fe2++2NO2↑+4H2O 2AlO
2AlO Al3++2H2O
Al3++2H2O