|
某溶液中可能含有Na+、NH4+、Ba2+、SO42-、I-、S2-.分别取样:①用pH计测试,溶液显弱酸性;②加氯水和淀粉无明显现象.为确定该溶液的组成,还需检验的离子是 | |
| [ ] | |
A. |
Na+ |
B. |
SO42- |
C. |
Ba2+ |
D. |
NH4+ |
|
根据碘与氢气反应的热化学方程式 (ⅰ)I2(g)+H2(g) (ⅱ)I2(S)+H2(g) 下列判断正确的是 | |
| [ ] | |
A. |
254 g I2(g)中通入2 g H2(g),反应放热9.48 kJ |
B. |
1 mol固态碘与1 mol气态碘所含的能量相差17.00 kJ |
C. |
反应(ⅰ)的产物比反应(ⅱ)的产物稳定 |
D. |
反应(ⅱ)的反应物总能量比反应(ⅰ)的反应物总能量低 |
|
用NA表示阿伏加德罗常数的值.下列叙述正确的是 | |
| [ ] | |
A. |
25℃时,pH=13的1.0 L Ba(OH)2溶液中含有的OH-数目为0.2NA |
B. |
标准状况下,2.24 L Cl2与过量稀NaOH溶液反应,转移的电子总数为0.2NA |
C. |
室温下,21.0 g乙烯和丁烯的混合气体中含有的碳原子数目为1.5NA |
D. |
标准状况下,22.4 L甲醇中含有的氧原子数为1.0NA |
|
14 C是碳的一种同位素,NA为阿伏加德罗常数,下列说法不正确的是①1 mol 14CH4分子中所含中子数为8NA ②7 g 14C原子形成的石墨中所含质子数为3NA ③17 g甲基(-14CH3)所含电子数为8NA ④常温常压下22.4 L 14CO2的分子数为NA | |
| [ ] | |
A. |
①② |
B. |
①③ |
C. |
①②③ |
D. |
③④ |
|
下列叙述中正确的是 ①标准状况下,1 L HCl和1 L H2O的物质的量相同; ②标准状况下,1 g H2和14 g N2的体积相同; ③28 g CO的体积为22.4 L; ④两种物质的物质的量相同,则它们在标准状况下的体积也相同; ⑤在同温同体积时,气体物质的物质的量越大,则压强越大; ⑥同温同压下,气体的密度与气体的相对分子质量成正比. | |
| [ ] | |
A. |
①②③ |
B. |
②⑤⑥ |
C. |
②③⑥ |
D. |
④⑤⑥ |
|
T℃时,在2 L密闭容器中X(g)与Y(g)反应生成Z(g),浓度变化如图1所示;若其他条件不变,温度为T1和T2时Y的体积百分含量与时间关系如图2所示.下列结论正确的是
| |
| [ ] | |
A. |
容器中的反应可表示为:3X(g)+Y(g)=2Z(g) |
B. |
图1中,前3 min内X的反应速率为v(X)=0.2 mol/(L·min) |
C. |
X与Y生成Z的反应为吸热反应 |
D. |
如果将容器的体积压缩为1 L,X的转化率将会减小 |
|
已知:2CH3OH(g)
下列说法正确的是 | |
| [ ] | |
A. |
平衡后升高温度,K>400 |
B. |
平衡时,c(CH3OCH3)=1.6 mol/L |
C. |
平衡时,反应混合物的总能量减少20 kJ |
D. |
平衡时,再加入与起始等量的CH3OH,达新平衡后CH3OH转化率增大 |
|
在体积为VL的恒容密闭容器中盛有一定量H2,通入Br2(g)发生反应:H2(g)+Br2(g)
| |
| [ ] | |
A. |
由图可知:T2>T1 |
B. |
两点的反应速率:a>b |
C. |
T1时,随着Br2(g)加入,平衡时HBr的体积分数不断增加 |
D. |
为了提高Br2(g)的转化率,可采取将HBr液化并及时移走的方法 |
|
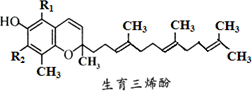
生育三烯酚的通式如下图,它有α、β、γ和δ四种结构,R1、R2代表的原子或原子团如下表.下列叙述中不正确的是
| |
| [ ] | |
A. |
α、δ两种生育三烯酚互为同系物,β和γ两种生育三烯酚互为同分异构体 |
B. |
四种生育三烯酚均可使溴水及酸性高锰酸钾溶液褪色,与FeCl3溶液发生显色反应 |
C. |
生育三烯酚的结构中存在异戊二烯的链节结构 |
D. |
1 mol γ-生育三烯酚与溴水发生反应,理论上最多可消耗5 mol Br2 |
 2HI(g)+9.48 kJ
2HI(g)+9.48 kJ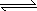 2HI(g)-26.48 kJ
2HI(g)-26.48 kJ
 CH3OCH3(g)+H2O(g);ΔH=-25 kJ/mol.某温度下的平衡常数K=400.已知平衡常数K=
CH3OCH3(g)+H2O(g);ΔH=-25 kJ/mol.某温度下的平衡常数K=400.已知平衡常数K= 2HBr(g);ΔH<0.当温度分别为T1、T2平衡时,H2的体积分数与Br2(g)的物质的量变化关系如图所示.下列说法正确的是
2HBr(g);ΔH<0.当温度分别为T1、T2平衡时,H2的体积分数与Br2(g)的物质的量变化关系如图所示.下列说法正确的是