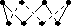|
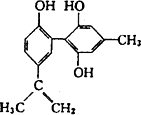
某种兴奋剂的结构简式如图所示,有关该物质的说法中的是
| |
| [ ] | |
A. |
遇FeCl3溶液显紫色,因为该物质与苯酚属于同系物 |
B. |
该分子中的所有原子不可能共平面 |
C. |
该物质能与浓溴水发生加成反应和取代反应 |
D. |
1 mol该物质在催化剂作用下最多能与7 mol H2发生加成反应 |
|
下列溶液中微粒浓度关系一定正确的是 | |
| [ ] | |
A. |
pH=4的盐酸与pH=10的氨水溶液等体积混合后pH>7 |
B. |
氯水中:c(Cl2)=2[c(ClO-)+c(Cl-)+c(HClO)] |
C. |
pH=11的NaOH和pH=11的氨水分别稀释100倍后的pH前者一定大于后者 |
D. |
0.10 mol·L-1 Na2CO3溶液:c(Na+)+c(H+)=c(OH-)+c(HCO |
|
常温下,下列各组离子在指定溶液中能大量共存的是 | |
| [ ] | |
A. |
c(SO |
B. |
pH=1的溶液中:NH |
C. |
强碱性溶液中:Na+、AlO |
D. |
水电离产生的c(H+)=1×10-14 mol·L-1的溶液中:HCO |
|
NA表示阿伏加德罗常数,下列叙述正确的是 | |
| [ ] | |
A. |
32 g S8单质(下图)中含有的S-S键个数为8 NA
|
B. |
常温下,16 g O2和O3的混合气体中所含氧原子数为2.5 NA |
C. |
1 mol Mg在空气中完全反应生成MgO、Mg3N2转移电子数为2 NA |
D. |
标准状况下,11.2 L的乙烯中含有的共用电子对数为NA |
|
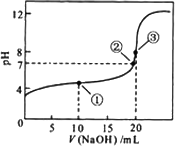
常温下 ,用0.1000 mol·L-1 NaOH溶液滴定20.00 mL 0.1000 mol·L-1 CH3COOH溶液所得滴定曲线如下图.下列说法正确的是
| |
| [ ] | |
A. |
点 ①所示溶液中:c(CH3COO-)+c(OH-)=c(CH3COOH)+c(H+) |
B. |
点 ②所示溶液中:c(Na+)=c(CH3COOH)+c(CH3COO-) |
C. |
点 ③所示溶液中:c(Na+)>c(OH-)>c(CH3COO-)>c(H+) |
D. |
滴定过程中可能出现:c(CH3COOH)>c(CH3COO-)>c(H+)>c(Na+)>c(OH-) |
|
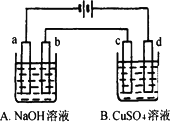
按下图装置进行电解(均是惰性电极),已知A烧杯中装有500 mL 20%的NaOH溶液,B烧杯中装有500 mL pH为6的1 mol·L-1 CuSO4溶液.通电一段时间后,在b电极上收集到28 mL气体(标准状况),则B烧杯中溶液pH变为(溶液体积变化忽略不计)
| |
| [ ] | |
A. |
4 |
B. |
3 |
C. |
2 |
D. |
1 |
|
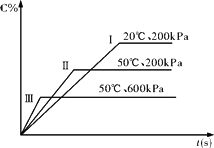
在密闭容器中进行以下可逆反应:A(g)+B(g)
| |
| [ ] | |
A. |
正反应放热,D是固体 |
B. |
正反应放热,D是气体 |
C. |
正反应吸热,D是气体 |
D. |
正反应放热,D是固体或气体 |
|
W、X、Y是原子序数依次增大的同一短周期元素.W、X是金属元素,它们的最高价氧化物的水化物之间可以反应生成盐和水;Y的最外层电子数是核外电子层数的2倍,W与Y可形成化合物W2Y.下列说法正确的是 | |
| [ ] | |
A. |
Y的低价氧化物与O3漂白的原理相同 |
B. |
Y的氢化物和W2Y所含化学键的类型相同 |
C. |
上述三种元素形成的简单离子,X离子半径最小 |
D. |
工业上常用电解相应的盐溶液制备W、X的单质 |
|
某氨水的pH=a,某盐酸的pH=b,已知a+b=14,将上述氨水与盐酸等体积混合后,所得溶液中各种离子浓度的关系正确的是 | |
| [ ] | |
A. |
c(
NH |
B. |
c(
Cl-)
>c(
NH |
C. |
c(
Cl-)
>c(
NH |
D. |
c(
NH |