|
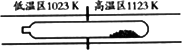
难挥发性二硫化钽(TaS2)可采用如下装置提纯.将不纯的TaS2粉末装入石英管一端,抽真空后引入适量碘并封管,置于加热炉中.反应如下: TaS2(s)+2I2(g)
| |
| [ ] | |
A. |
在不同温度区域,TaI4的量保持不变 |
B. |
在提纯过程中,I2的量不断减少 |
C. |
在提纯过程中,I2的作用是将TaS2从高温区转移到低温区 |
D. |
该反应的平衡常数与TaI4和S2的浓度乘积成反比 |
|
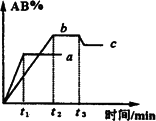
在一定条件下,反应A2+B2
| |
| [ ] | |
A. |
AB可能为气体 |
B. |
A2与B2都为气体 |
C. |
Q>0 |
D. |
Q<0 |
|
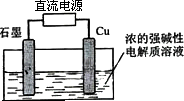
Cu2O 是一种半导体材料,基于绿色化学理念设计的制取Cu2O的电解池示意图如下,电解总反应:2Cu+H2O=Cu2O+H2↑.下列说法正确的是
| |
| [ ] | |
A. |
石墨电极上产生Cu2O |
B. |
铜电极发生还原反应 |
C. |
铜电极接直流电源的负极 |
D. |
当有0.1 mol电子转移时,有0.05 mol Cu2O生成. |
|
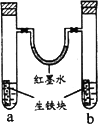
下图装置中,U型管内为红墨水,a、b试管内分别盛有食盐水和氯化铵溶液,各加入生铁块,放置一段时间.下列有关描述正确的是
| |
| [ ] | |
A. |
生铁块中的碳是原电池的负极 |
B. |
红墨水柱两边的液面变为左低右高 |
C. |
两试管中相同的电极反应式是:Fe-2e-=Fe2 + |
D. |
a试管中发生了析氢腐蚀,b试管中发生了吸氧腐蚀 |
|
通常情况下,将pH分别为8和10的两种NaOH溶液等体积混合,混合溶液的C(H +)最接近于 | |
| [ ] | |
A. |
1×(10-8+10-10)mol/L |
B. |
|
C. |
1×(10-14-5×10-5)mol/L |
D. |
2×10-10 mol/L |
|
下列说法正确的是 | |
| [ ] | |
A. |
向 0.1 mol/L Na2CO3溶液中滴加酚酞,溶液变红 |
B. |
Al3+ 、NO |
C. |
乙醇和乙酸都能溶于水,都是电解质 |
D. |
分别与等物质的量的HCl和H2SO4反应时,消耗NaOH的物质的量相同 |
|
物质的量浓度相同的下列溶液,pH由大到小排列正确的是 | |
| [ ] | |
A. |
Ba(OH)2 、Na2SO3、FeCl3、KCl |
B. |
Na2SiO3 、Na2SO3、KNO3、NH4Cl |
C. |
NH3·H2O 、H3PO4、Na2SO4、H2SO4 |
D. |
NaHCO3 、C6H5COOH、C2H5OH、HCl |
|
向一定量的Fe、FeO和Fe2O3的混合物中加入120 mL 4 mol/L的稀硝酸,恰好使混合物完全溶解,放出1.344 L NO(标准状况),往所得溶液中加入KSCN溶液,无血红色出现.若用足量的氢气在加热下还原相同质量的混合物,能得到铁的物质的量为: | |
| [ ] | |
A. |
0.24 mol |
B. |
0.21 mol |
C. |
0.16 mol |
D. |
0.14 mol |
|
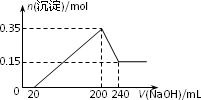
将一定质量的镁和铝混合物投入200 mL硫酸中,固体全部溶解后,向所得溶液中加入NaOH溶液,生成沉淀的物质的量n与加入NaOH溶液的体积V的变化如下图所示.则下列说法不正确的是:
| |
| [ ] | |
A. |
生成的氢气在标准状况下的体积为11.2 L |
B. |
最初20 mL NaOH溶液用于中和过量的硫酸 |
C. |
硫酸的物质的量浓度为2.5 mol·L–1 |
D. |
镁和铝的总质量为9 g |
|
下列各组离子一定能大量共存的是: | |
| [ ] | |
A. |
在含有大量AlO2-的溶液中:NH4 +、Na+、Cl-、H+ |
B. |
在强碱溶液中:Na +、K+、CO32-、NO3- |
C. |
在pH=13的溶液中:NH4 +、Na+、SO42-、Cl- |
D. |
在c(H +)=0.1mol·L-1的溶液中:K+、I-、Cl-、NO3- |