|
下列离子方程式书写正确的是: | |
| [ ] | |
A. |
用铂电极电解氯化镁溶液:Cl-+2H2O |
B. |
NaHSO4溶液中滴入Ba(OH)2溶液至中性:H++SO42-+Ba2+十OH- |
C. |
在H2O2中加入酸性KMnO4溶液:2MnO4-+5H2O2+6H+ |
D. |
溴乙烷与6 mol/L氢氧化钠水溶液共热:C2H5Br+OH- |
|
铁溶于一定浓度的硝酸溶液时,发生反应的离子方程式为: aFe+bNO3-+cH+ 下列有关推断中,不正确的是 | |
| [ ] | |
A. |
2d+3f=3g+h |
B. |
反应中每消耗5.6 g Fe,转移0.2 mol~0.3 mol e- |
C. |
HNO3的氧化性大于Fe3+ |
D. |
当a不变时,d随着b的增大而增大 |
|
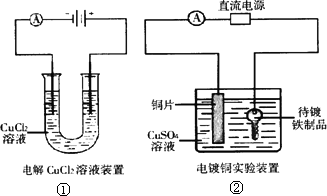
关于下列各图的说法,正确的是
| |
| [ ] | |
A. |
①装置中阴极处产生的气体能够使湿润淀粉KI试纸变蓝 |
B. |
②装置中待镀铁制品应与电源正极相连 |
C. |
③装置中电子由b极流向a极 |
D. |
④装置中的离子交换膜可以避免生成的Cl2与NaOH溶液反应 |
|
设NA为阿伏加德罗常数,下列说法正确的是 | |
| [ ] | |
A. |
标准状况下,5.6 L四氯化碳含有的分子数为0.25NA |
B. |
标准状况下,14 g氮气含有的核外电子数为5NA |
C. |
标准状况下,22.4 L任意比的氢气和氯气的混合气体中含有的分子总数均为NA |
D. |
标准状况下,铝跟氢氧化钠溶液反应生成1 mol氢气时,转移的电子数为NA |
|
在指定环境中,下列各组离子一定可以大量共存的是 | |
| [ ] | |
A. |
使pH试纸呈红色的溶液中:Fe2+、NO3-、SO42-、Na+ |
B. |
滴加无色酚酞试液后仍无色的溶液中:CO32-、K+、ClO-、AlO2- |
C. |
在c(H+)/c(OH-)=1×1013的溶液中:NH4+、Ca2+、C1-、K+ |
D. |
加入铝粉后产生大量氢气的溶液中:NH4+、Na+、NO3-、SO42- |
|
神舟七号”宇宙飞船的能量部分来自太阳能电池,另外内部还配有高效的MCFC型燃料电池.该电池可同时供应电和水蒸气,所用燃料为氢气,电解质为熔融的碳酸钾.已知该电池的总反应为2H2+O2 | |
| [ ] | |
A. |
电池工作时,CO32-向负极移动 |
B. |
电池放电时,外电路电子由通氧气的正极流向通氢气的负极 |
C. |
正极的电极反应为:4OH-→O2↑+2H2O+2e- |
D. |
通氧气的电极为阳极,发生氧化反应 |
|
下列各组离子,因氧化还原反应而不能大量共存的是 | |
| [ ] | |
A. |
K+、Na+、Cl-、NO3- |
B. |
H+、Na+、NO3-、I- |
C. |
K+、Ba2+、SO42-、NO3- |
D. |
H+、Na+、CO32-、Cl- |
|
有五瓶溶液分别是:①10 mL 0.60 mol/L NaOH水溶液;②20 mL 0.50 mol/L硫酸溶液;③30 mL 0.40 mol/L HCl溶液;④40 mL 0.30 mol/L CH3COOH水溶液;⑤50 mL 0.20 mol/L蔗糖水溶液.以上各瓶溶液所含离子、分子总数的大小顺序是 | |
| [ ] | |
A. |
①>②>③>④>⑤ |
B. |
②>①>③>④>⑤ |
C. |
②>③>④>①>⑤ |
D. |
⑤>④>③>②>① |
|
高铁电池是一种新型可充电电池,与普通高能电池相比,该电池能长时间保持稳定的放电电压.高铁电池的总反应为3Zn+2K2FeO4+8H2O 下列叙述不正确的是 | |
| [ ] | |
A. |
放电时负极反应为:Zn-2e-+2OH- |
B. |
充电时阳极反应为:Fe(OH)3-3e-+5OH- |
C. |
放电时每转移3 mol电子,正极有1 mol K2FeO4被氧化 |
D. |
放电时正极附近溶液的碱性增强 |
|
下表为元素周期表中短周期的一部分.下列有关A、B、C、D、E五种元素的叙述中,不正确的是
| |
| [ ] | |
A. |
A与B形成的阴离子可能有:AB32-、A2B42- |
B. |
C的氢化物的沸点比E的氢化物的沸点高 |
C. |
D在过量的B中燃烧的主要产物为DB3 |
D. |
由这5种元素中的几种形成只含极性键的非极性分子不少于4种 |