|
高铁酸钾是一种理想的绿色水处理剂,工业上可通过如下反应制得 2Fe(OH)3+3ClO-+4OH-=2FeO42-+3C1-+5H2O 在上述反应中 | |
| [ ] | |
A. |
FeO42-是还原产物 |
B. |
CIO-是还原剂 |
C. |
1 mol Fe(OH)3失去3 mol电子 |
D. |
没有电子得失 |
|
下列各组离子中,在碱性溶液中能共存,且加入盐酸过程中会产生气体和沉淀的是 | |
| [ ] | |
A. |
Na+、NO3-、AlO2-、SO42- |
B. |
Na+、NO3-、SiO32-、K+ |
C. |
K+、Cl-、AlO2-、CO32- |
D. |
Na+、Cl-、HCO3-、Ca2+ |
|
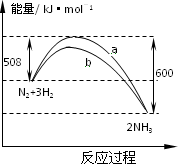
下图是198 K时N2与H2反应过程中能量变化的曲线图.下列叙述正确的是
| |
| [ ] | |
A. |
该反应的热化学方程式为: N2+3H2 |
B. |
b曲线是加入铁触媒时的能量变化曲线 |
C. |
加入铁触媒,该化学反应的反应热改变 |
D. |
加入铁触媒可增大正反应速率,降低逆反应速率,反应物的转化率提高 |
|
设NA为阿伏加德罗常数,下列说法正确的是 | |
| [ ] | |
A. |
1 mol甲基正离子(CH3+)所含电子数为8NA |
B. |
标准状况下将0.5 mol SO2气体与0.5 mol H2S气体混合后,气体的分子总数为NA |
C. |
500 mL 0.5 mol/L的Ca(ClO)2溶液中,含有ClO-的数目为0.5NA |
D. |
31 g白磷分子中有NA个P-P键 |
|
下列反应的离子方程式书写正确的是 | |
| [ ] | |
A. |
向NH4HSO4稀溶液中逐滴加入Ba(OH)2稀溶液至刚好沉淀完全: Ba2++2OH-+NH4++H++SO42-=BaSO4↓+NH3·H2O+H2O |
B. |
碳酸钙溶于醋酸:CaCO3+2H+ |
C. |
向硅酸钠溶液中通入过量的CO2: SiO32-+CO2+H2O=H2SiO3↓+CO32- |
D. |
澄清石灰水与少量苏打溶液混合: Ca2++OH-+HCO3- |
|
要提纯下列物质(括号内物质为杂质),实验操作最合理的是 | |
| [ ] | |
A. |
CO2(SO2):通入盛有品红溶液的洗气瓶后收集 |
B. |
Fe2+(Fe3+):加KSCN溶液后过滤 |
C. |
Cl2(HCl):通过盛有饱和氯化钠水溶液的洗气瓶后收集 |
D. |
氯化铵溶液(FeCl3):加足量NaOH溶液后过滤 |
|
物质氧化性、还原性的强弱,不仅与物质的结构有关,还与物质的浓度和反应温度等有关.下列各组物质: ①Cu与浓硝酸 ②Fe与浓硫酸 ③Na与氧气 ④P2O5与水 由于反应温度不同而能发生不同氧化还原反应的是 | |
| [ ] | |
A. |
②③④ |
B. |
②③ |
C. |
①②③ |
D. |
③④ |