|
下列叙述中正确的是 | |
| [ ] | |
A. |
1 moL CO和1 mol N2所含分子数相等,质量也相等,所以他们所占的体积也一定相同 |
B. |
等体积、等物质的量浓度的强碱溶液中,所含的OH-数一定相等 |
C. |
22.4 L H2和71 g Cl2反应,恰好生成2 mol HCl |
D. |
非标准状况下,1 mol某气体的体积可能是22.4 L |
|
一定条件下,用甲烷可以消除氮氧化物(NO2)的污染.已知: ①CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g);ΔH=-574 kJ·mol-1 ②CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g);ΔH=-1160 kJ·mol一1. 下列选项正确的是 | |
| [ ] | |
A. |
CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(l);ΔH=-867 kJ·mol-1 |
B. |
若0.2 mol CH4还原NO2至N2,在上述条件下放出的热量为173.4 kJ |
C. |
CH4催化还原NOx为N2的过程中,若x=1.6,则转移的电子为3.2 mol |
D. |
若用标准状况下2.24 L CH4还原NO2至N2,整个过程中转移的电子为1.6 mol |
|
下列各组物质稀溶液相互反应,无论前者滴入后者,还是后者滴入前者,反应现象相同,且离子方程相同的是 | |
| [ ] | |
A. |
Ba(HCO3)2溶液和Ba(OH)2溶液 |
B. |
NaAlO2溶液与稀硫酸溶液 |
C. |
Ca(HCO3)2溶液和NaOH溶液 |
D. |
氨水与硝酸银溶液 |
|
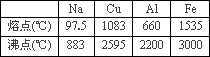
所谓合金,就是不同种金属(也包括一些非金属)在熔融状态下形成的一种熔合物,根据下列四种金属的熔、沸点,判断其中不能形成合金的是
| |
| [ ] | |
A. |
Cu和Al |
B. |
Fe和Cu |
C. |
Fe和Na |
D. |
Al和Na |
|
将Mg、Cu组成的混合物26.4 g投入到适量的稀硝酸中,固体完全溶解,收集到标准状况下的NO气体8.96 L,向反应后的溶液中加入过量的5 mol·L-1的NaOH溶液300 mL,金属离子完全沉淀.则形成沉淀的质量是 | |
| [ ] | |
A. |
43.2 g |
B. |
46.8 g |
C. |
53.6 g |
D. |
63.8 g |
|
NA代表阿伏加德罗常数,下列说法正确的是 | |
| [ ] | |
A. |
在同温同压时,相同体积的任何气体单质所含的原子数目相同 |
B. |
2 g氢气所含原子数目为NA |
C. |
在常温常压下,11.2 L氮气所含的原子数目为NA |
D. |
17 g氨气所含电子数目为NA |
|
下列反应的离子方程式书写正确的是 | |
| [ ] | |
A. |
氢氧化钠溶液中通少量二氧化硫: |
B. |
碳酸氢钠溶液与足量氢氧化钡溶液混合 |
C. |
盐酸滴入氨水中:H++OH-=H2O |
D. |
碳酸钙溶液于稀硝酸中: |
|
下列各组离子能在指定环境中大量共存的是 | |
| [ ] | |
A. |
在c(HCO |
B. |
在由水电离出的c(H)+=1×10-12 mol/L的溶液中 |
C. |
PH=1的溶液中Mg2+,Fe2+,NO |
D. |
在使红色石蕊试纸变蓝的溶液中 |