|
关于Na2CO3溶液和NaHCO3溶液,下列说法正确的是 | |
| [ ] | |
A. |
用加热的方法区别两种溶液 |
B. |
用澄清的石灰水区别两种溶液 |
C. |
浓度相同时,Na2CO3溶液的pH大 |
D. |
浓度相同时,两溶液的pH相等 |
|
向50 mL 18 mol/L H2SO4溶液中加入足量的铜片并加热,充分反应后,被还原的H2SO4的物质的量 | |
| [ ] | |
A. |
小于0.45 mol |
B. |
等于0.45 mol |
C. |
在0.45 mol和0.90 mol之间 |
D. |
大于0.90 mol |
|
下列离子方程式正确的是 | |
| [ ] | |
A. |
氢氧化铁溶于氢碘酸中:Fe(OH)3+3H+=Fe3++3H2O |
B. |
明矾溶液中加入氢氧化钡溶液,使其产生沉淀的物质的量达最大值: Al3++2SO42-+2Ba2++4OH-=2BaSO4↓+AlO2-+2H2O |
C. |
Mg(HCO3)2溶液中加入过量石灰水: Mg2++2HCO3-+Ca2++2OH-=CaCO3↓+2H2O+MgCO3↓ |
D. |
向100 mL 0.1 mol/L的FeBr2溶液中通入0.012 mol Cl2: 10Fe2++14Br-+12Cl2=10Fe3++7Br2+24Cl- |
|
对于反应4FeS2+11O2 | |
| [ ] | |
A. |
铁和硫两种元素被还原 |
B. |
只有硫元素被氧化 |
C. |
转移电子总数是44e- |
D. |
Fe2O3为氧化产物,SO2为还原产物 |
|
根据下列四个反应方程式判断:氧化性由强到弱的顺序正确的是 ①2A-+B2= ②2A-+C2= ③2B-+C2= ④2C-+D2= | |
| [ ] | |
A. |
D2>C2>B2>A2 |
B. |
A2>B2>C2>D2 |
C. |
C2>A2>B2>D2 |
D. |
B2>D2>C2>A2 |
|
0.1 mol/L NaOH溶液和0.1 mol/L NH4Cl溶液等体积混合后,溶液中离子浓度大小顺序正确的是 | |
| [ ] | |
A. |
c(Na+)>c(Cl-)>c(OH-)>c(H+) |
B. |
c(Na+)=c(Cl-)>c(H+)>c(OH-) |
C. |
c(Na+)=c(Cl-)>c(OH-)>c(H+) |
D. |
c(Cl-)>c(Na+)>c(OH-)>c(H+) |
|
在由水电离产生的H+浓度为1×10-13 mol/L的溶液中,一定能大量共存的离子组是 ①K+、Cl-、NO3-、S2- ②K+、Fe2+、I-、SO42- ③Na+、Cl-、NO3-、SO42- ④Na+、Ca2+、Cl-、HCO3- ⑤K+、Ba2+、Cl-、NO3- | |
| [ ] | |
A. |
①③ |
B. |
③⑤ |
C. |
③④ |
D. |
②⑤ |

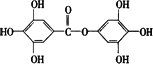 ,1 mol A与足量的NaOH溶液混合共热,充分反应后最多消耗NaOH的物质的量为
,1 mol A与足量的NaOH溶液混合共热,充分反应后最多消耗NaOH的物质的量为