|
下列除去杂质的方法正确的是 | |
| [ ] | |
A. |
除去N2中的少量O2:通过灼热的CuO粉末,收集气体 |
B. |
除去CO2中的少量HCl:通入Na2CO3溶液,收集气体 |
C. |
除去FeCl2溶液中的少量FeCl3:加入足量铁屑,充分反应后,过滤 |
D. |
除去KCl溶液中的少量MgCl2:加入适量NaOH溶液,过滤 |
|
水资源非常重要,联合国确定2003年为国际淡水年.下列关于水的说法中错误的是 | |
| [ ] | |
A. |
蒸馏法是海水淡化的方法之一 |
B. |
淡水的密度小于海水的密度 |
C. |
融化的雪水中矿物质含量比深井水中的少 |
D. |
0℃以上,温度越高,水的密度越小 |
|
制备氰氨基化钙的化学方程式为 CaCO3+2HCN | |
| [ ] | |
A. |
氢元素被氧化,碳元素被还原 |
B. |
HCN既是氧化剂又是还原剂 |
C. |
CaCN2是还原产物,H2是氧化产物 |
D. |
CO是氧化产物,H2是还原产物 |
|
利尿剂是2008北京奥运会违禁药物,顾名思义,此类药物有稀释尿液的功能.利尿剂现有15种,主要用于掩盖或“清洗”体内其他违禁药品的存在,以逃避兴奋剂检查.利尿酸是其中之一,其结构简式为:
下列叙述正确的是 | |
| [ ] | |
A. |
1 mol利尿酸最多可与5 mol H2发生加成反应 |
B. |
利尿酸分子中位于同一平面内的原子有10个 |
C. |
利尿酸分子式是C11H12O4 |
D. |
利尿酸与新制Cu(OH)2悬浊液反应有红色沉淀生成 |
|
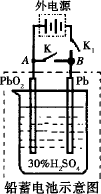
铅蓄电池是典型的可充电电池,它的正负极隔板是惰性材料,电池总反应式为:
| |
| [ ] | |
A. |
放电时负极反应是:Pb-2e- |
B. |
闭合K断开K1,电流的流动方向是从B到A |
C. |
放电过程中,溶液的pH不断减小 |
D. |
放电时,线路上若有1 mol e-通过,则消耗硫酸也是1 mol |
|
现有t℃时质量分数为a%的KNO3溶液m g,将其分成质量比为1∶2的甲、乙两份溶液.甲溶液蒸发5 g水,恢复到原温度时析出晶体2 g;乙溶液蒸发12 g水,恢复到原温度时析出晶体5 g.则t℃时,KNO3溶解度为 | |
| [ ] | |
A. |
41.7 g |
B. |
50 g |
C. |
42.9 g |
D. |
60 g |
|
下列指定条件下的结论正确的是 | |
| [ ] | |
A. |
|
B. |
10 mL 0.02 mol·L-1 HCl溶液与10 mL 0.02 mol·L-1 Ba(OH)2溶液充分混合,若混合后溶液的体积为20 mL,则溶液的pH=7 |
C. |
在0.1 mol·L-1 CH3COONa溶液中,c(OH-)=c(CH3COOH)+c(H+) |
D. |
0.1 mol·L-1某二元弱酸盐NaHA溶液中,c(Na+)=2c(A2-)+c(HA-)+c(H2A) |
|
“类推”是一种常用的学习方法,但有时类推会产生错误的结论,下列类推结论中正确的是 | |
| [ ] | |
A. |
NH4Cl加热分解只生成HCl和NH3,NH4I固体加热分解也只生成HI和NH3 |
B. |
第二周期元素氢化物的稳定性顺序是:HF>H2O>NH3,则第三周期元素氢化物的稳定性顺序也是:HCl>H2S>PH3 |
C. |
溶液中有阳离子,必有阴离子,则晶体中有阳离子,必有阴离子 |
D. |
干冰(CO2)是分子晶体,则SiO2也是分子晶体 |
|
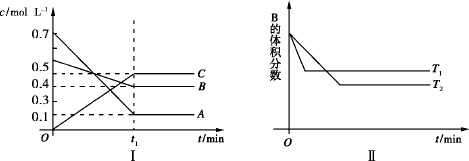
T℃时,反应物和生成物均为气体的某反应,反应过程中浓度变化如下图(Ⅰ)所示.若保持其他条件不变,温度分别为T1和T2时,B的体积分数与时间的关系如下图(Ⅱ)所示,则下列结论正确的是
| |
| [ ] | |
A. |
在t1时间内用B表示该反应的平均速率为:0.6 mol·L-1·min-1 |
B. |
在(t1+10)时,保持其他条件不变,增大压强,平衡向逆反应方向移动 |
C. |
T℃时,在相同容器中,若由0.1 mol·L-1 A、0.3 mol·L-1 B和0.4 mol·L-1 C反应,达到平衡后,C的浓度仍为0.4 mol·L-1 |
D. |
在其他条件不变时,升高温度,正、逆反应速率均增大,且A的转化率增大 |