|
在100 mL混合溶液中,HNO3和H2SO4物质的量浓度分别为0.4 mol·L-1和0.1 mol·L-1,向该溶液中加入1.92 g铜粉,加热,待充分反应后,所得溶液中Cu2+物质的量浓度(mol·L-1)为 | |
| [ ] | |
A. |
0.15 |
B. |
0.20 |
C. |
0.225 |
D. |
0.45 |
|
为检验某病人血液中的含钙量,现取10 mL血液样品稀释后用草酸铵[(NH4)2C2O4]处理成草酸钙沉淀,将此沉淀溶于过量的稀H2SO4中,然后用0.5 mol·L KMnO4溶液滴定(生成Mn2+、CO2、H2O)恰好消耗1.6 mL,则该病人血液中含钙量为 | |
| [ ] | |
A. |
2.4 g/L |
B. |
8 g/L |
C. |
6 g/L |
D. |
12 g/L |
|
将一定体积的某NaOH溶液分成两等份,一份用pH=2的一元酸HA溶液中和,消耗酸溶液的体积为V1;另一份用pH=2的一元酸HB溶液中和,消耗酸溶液体积为V2,则下列叙述正确的是 | |
| [ ] | |
A. |
若V1>V2,则说明HA的酸性比HB的酸性强 |
B. |
若V1>V2,则说明HA的酸性比HB的酸性弱 |
C. |
因为两种酸溶液的pH相等,故V1一定等于V2 |
D. |
若将等体积的两种酸溶液分别与足量的锌反应,则所得氢气的体积一定相等 |
|
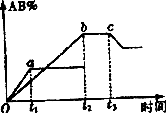
反应A2+B2
| |
| [ ] | |
A. |
A2、B2、AB均为气体,正反应放热 |
B. |
AB为固体,A2、B2中最少有一种为非气体,正反应吸热 |
C. |
AB为气体,A2、B2中最少有一种为非气体,正反应吸热 |
D. |
AB为气体,A2、B2中最少有一种为非气体,正反应放热 |
|
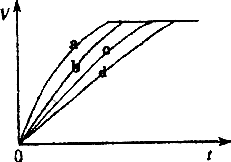
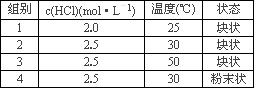
等质量的铁与过量的盐酸在不同的试验条件下进行反应,测定在不同时间t产生氢气体积V的数据,根据数据绘制得到下图,则曲线a、b、c、d所对应的试验组别可能是
| |
| [ ] | |
A. |
4-3-1-2 |
B. |
1-2-3-4 |
C. |
3-4-2-1 |
D. |
1-2-4-3 |
|
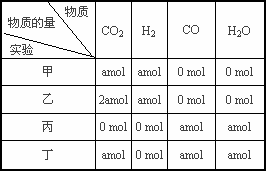
在相同温度和压强下,对反应CO2(g)+H2(g)
上述四种情况达到平衡后,n(CO)的大小顺序是 | |
| [ ] | |
A. |
乙=丁>丙=甲 |
B. |
乙>丁>甲>丙 |
C. |
丁>乙>丙=甲 |
D. |
丁>丙>乙>甲 |
|
镍镉(Ni-Cd)可充电电池在现代生活中有广泛应用.已知某镍镉电池的电解质溶液为KOH溶液,其充、放电按下式进行:Cd+2NiOOH+2H2O | |
| [ ] | |
A. |
充电时阳极反应:Ni(OH)2-e-+OH- |
B. |
充电过程是化学能转化为电能的过程 |
C. |
放电时负极附近溶液的碱性不变 |
D. |
放电时电解质溶液中的OH-向正极移动 |
|
用石墨电极电解硝酸银溶液,在阳极收集到0.40克氧气,中和电解时生成的酸需要250毫升氢氧化钠溶液,则氢氧化钠溶液的浓度是 | |
| [ ] | |
A. |
0.20摩/升 |
B. |
0.15摩/升 |
C. |
0.10摩/升 |
D. |
0.05摩/升 |
|
下列有关金属腐蚀与防护的说法正确的是 | |
| [ ] | |
A. |
将青铜器放在银质托盘上可以避免生成铜绿 |
B. |
当镀锡铁制品的镀层破损时,镶层仍能对铁制品起保护作用 |
C. |
在海轮外壳连接锌块保护外壳不受腐蚀是采用了牺牲阳极的阴极保护法 |
D. |
可将地下输油钢管与外加直流电源的正极相连以保护它不受腐蚀 |