|
绿色化学的核心就是利用化学原理从源头上减少和消除工业生产对环境的污染.下列做法不符合绿色化学理念的是 | |
| [ ] | |
A. |
研制水溶剂涂料替代有机溶剂涂料 |
B. |
用可降解塑料生产包装盒或快餐盒 |
C. |
用反应:Cu+2H2SO4(浓) |
D. |
用反应:2CH2=CH2+O2 |
|
氢化钙可以作为生氢剂(其中CaH2中氢元素为-1价),反应方程式如下:CaH2+2H2O=Ca(OH)2+2H2↑,其中水的作用是 | |
| [ ] | |
A. |
既不是氧化剂也不是还原剂 |
B. |
是氧化剂 |
C. |
是还原剂 |
D. |
既是氧化剂又是还原剂 |
|
下列离子方程式中正确的是 | |
| [ ] | |
A. |
硫酸镁溶液和氢氧化钡溶液反应SO42-+Ba2+ |
B. |
铜片加入稀硝酸中:Cu+2NO3-+4H+ |
C. |
FeBr2溶液中加入过量的氯水2Fe2++2Br-+2Cl2 |
D. |
等体积等物质的量浓度的NaHCO3和Ba(OH)2两溶液混合: HCO3-+Ba2++OH- |
|
下列条件下,两瓶气体所含原子数一定相等的是 | |
| [ ] | |
A. |
同质量、不同密度的N2和CO |
B. |
同温度、同体积的H2和N2 |
C. |
同体积、不同密度的C2H4和C3H6 |
D. |
同压强、同体积的N2O和CO2 |
|
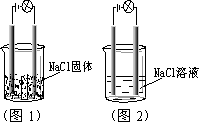
一化学兴趣小组在家中进行化学实验,按照图1连接好线路发现灯泡不亮,按照图2连接好线路发现灯泡亮,由此得出的结论正确的是
| |
| [ ] | |
A. |
NaCl是非电解质 |
B. |
NaCl溶液是电解质 |
C. |
NaCl在水溶液中电离出了可以自由移动的离子 |
D. |
NaCl溶液中水电离出大量的离子 |
|
在配制一定物质的量浓度的盐酸溶液时,下列错误操作可使所配制溶液浓度偏高的是 | |
| [ ] | |
A. |
用量筒量取浓盐酸时俯视读数 |
B. |
溶解搅拌时有液体飞溅 |
C. |
定容时俯视容量瓶瓶颈刻度线 |
D. |
摇匀后见液面下降,再加水至刻度线 |
|
下列叙述正确的是 | |
| [ ] | |
A. |
在氧化还原反应中,肯定有一种元素被氧化,另一种元素被还原 |
B. |
有单质参加的反应一定是氧化还原反应 |
C. |
有单质参加的化合反应一定是氧化还原反应 |
D. |
失电子难的原子,容易获得的电子 |
|
关于胶体和溶液的叙述中正确的是 | |
| [ ] | |
A. |
胶体带电荷,而溶液呈电中性 |
B. |
胶体加入某些盐可产生沉淀,而溶液不能 |
C. |
胶体是一种介稳性的分散系,而溶液是一种非常稳定的分散系 |
D. |
胶体能够发生丁达尔现象,溶液也能发生丁达尔现象 |
|
设NA代表阿伏加德罗常数,下列说法正确的是 | |
| [ ] | |
A. |
5.6 g铁与足量盐酸反应转移的电子数为0.3NA |
B. |
100 mL 2.0 mol/L的盐酸与醋酸溶液中氢离子均为0.2NA |
C. |
标准状况下,22.4 L氦气与22.4 L氟气所含原子数均为2NA |
D. |
常温常压下,20 g重水(D2O)中含有的电子数为10NA |
|
11.9 g锡与100 mL 12 mol·L-1 HNO3共热一段时间.完全反应后测定溶液中C(H+)为8 mol·L-1,溶液体积仍为100 mL.放出的气体在标准状况下体积约为8.96 L.由此推断氧化产物可是 | |
| [ ] | |
A. |
SnO2·4H2O |
B. |
Sn(NO3)4 |
C. |
Sn(NO3)2 |
D. |
Sn(NO3)2和Sn(NO3)4 |