|
一定能在下列溶液中大量共存的离子组是 | |
| [ ] | |
A. |
水电离产生的H+浓度为1×10-12 mol/L的溶液:NH |
B. |
能使pH试纸变深蓝色的溶液:Na+、AlO |
C. |
含有大量Fe3+的溶液:SCN-、I-、K+、Br- |
D. |
澄清透明的无色溶液:ClO-、MnO |
|
下列反应的离子方程式正确的是 | |
| [ ] | |
A. |
Fe3O4与稀硝酸反应 Fe3O4+8H+ |
B. |
向硝酸银溶液中逐滴滴入稀氨水直至过量:Ag++2NH3·H2O |
C. |
Ca(HCO3)2与过量Ca(OH)2溶液反应:Ca2++2HCO |
D. |
Na2S溶液呈碱性:S2-+2H2O |
|
MnO2和Zn是制造干电池的重要原料,工业上用软锰矿和闪锌矿联合生产MnO2和Zn的基本步骤为: (1)软锰矿、闪锌矿与硫酸共热:MnO2+ZnS+2H2SO4 (2)除去反应混合物中的不溶物 (3)电解混合液MnSO4+ZnSO4+2H2O 下列说法不正确的是 | |
| [ ] | |
A. |
步骤(1)中MnO2和H2SO4都是氧化剂 |
B. |
硫酸在生产中可循环使用 |
C. |
步骤(1)中每析出12.8 g S沉淀共转移0.8 mol电子 |
D. |
电解时MnO2在阳极处产生 |
|
下列离子方程式书写正确的是 | |
| [ ] | |
A. |
碳酸氢钙溶液中加入等物质的量的氢氧化钠溶液 Ca2++2HCO3-+2OH-=CaCO3↓+2H2O+CO32- |
B. |
氯化铝溶液中加入过量氨水Al3++3NH3·H2O=Al(OH)3↓+3NH4+ |
C. |
0.1 mol溴化亚铁中滴入含Cl2 0.1 mol氯水: 2Fe2++4Br-+3Cl2=2Fe3++2Br2+6Cl- |
D. |
浓盐酸跟二氧化锰混合共热MnO2+4H++4Cl- |
|
在某澄清、透明的浅黄色溶液中,可能含有下列八种离子:H+、NH4+、Fe3+、Ba2+、Al3+、SO42-、HCO3-、I-,在检验方案设计时初步分析其溶液中最多可含离子(不包括K+和OH-)有 | |
| [ ] | |
A. |
4种 |
B. |
5种 |
C. |
6种 |
D. |
7种 |
|
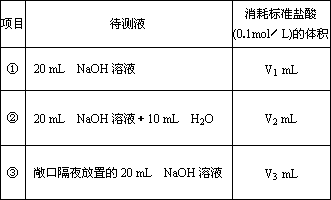
以酚酞试液为指示剂,对某新制的NaOH溶液进行中和滴定实验.数据记录如下表:
该新制的NaOH溶液的浓度c(NaOH)合理的是 | |
| [ ] | |
A. |
c(NaOH)=0.10×(V1+V2+V3)/(3×20)mol·L-1 |
B. |
c(NaOH)=0.10×(V1+V2)/(2×20)mol·L-1 |
C. |
c(NaOH)=0.10×(V1+V3)/(2×20)mol·L-1 |
D. |
c(NaOH)=0.10×V1/20 mol·L-1 |
|
中学化学实验中常见的使用温度计如下三种情况:①温度计的液泡浸没在液体反应物液面以下并接近容器的底部;②温度计的液泡置于水浴中;③温度计的液泡置于蒸馏烧瓶的支管处.下列实验使用温度计正确的是 | |
| [ ] | |
A. |
苯的硝化反应 ① |
B. |
酒精和浓硫酸混合加热制乙烯 ① |
C. |
测定硝酸钾在水中的溶解度 ③ |
D. |
分离苯和硝基苯的混合物 ② |
|
在硫酸铝、硫酸钾和明矾的混合溶液中,如果 | |
| [ ] | |
A. |
0.125 mol·L-1 |
B. |
0.225 mol·L-1 |
C. |
0.250 mol·L-1 |
D. |
0.450 mol·L-1 |