|
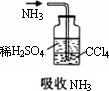
下列各组离子,在指定环境中一定能大量共存的是 | |
| [ ] | |
A. |
在pH>7的溶液中,Na+、S2-、K+、AlO2- |
B. |
在由水电离子的c(H+)=1×10-13 mol/L的溶液中,SO42-、S2-、K+、NH4+ |
C. |
溶解有Na2CO3的溶液中,Al3+、Cu2+、Cl-、NO3- |
D. |
在pH=0的溶液中,Fe2+、ClO-、Na+、SO42- |
|
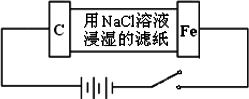
某同学设计一个如图所示(用铅蓄电池做电源)的电化学实验.下列说法正确的是
| |
| [ ] | |
A. |
电解池的阳极电极反应式:Fe-2e-=Fe2+ |
B. |
电解池的阴极电极反应式:2H++2e-=H2↑ |
C. |
铅蓄电池的负极的电极反应式:PbO2+4H++SO42-+2e-=PbSO4+2H2O |
D. |
铅蓄电池的负极的电极反应式:Pb-2e-=Pb2+ |
|
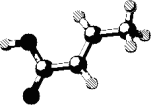
某有机物的分子结构如图(图中棍表示单键、双键或叁键),它属烃或烃的含氧衍生物.关于该有机物的叙述不正确的是
| |
| [ ] | |
A. |
该有机物的化学式为C4H6O2 |
B. |
该有机物可使溴水褪色,也可与NaOH溶液反应 |
C. |
该有机物可发生取代反应和加成反应 |
D. |
该有机物是乙酸的同系物 |
|
对于氧化还原反应:CuSO4+KI——K2SO4+CuI↓+I2,下列说法正确的是 | |
| [ ] | |
A. |
氧化剂和还原剂的物质的量之比1∶2 |
B. |
1 mol氧化剂在反应中得到的电子1 mol |
C. |
氧化产物与还原产物的物质的量之比为2∶1 |
D. |
该反应的离子方程式Cu2++3I-=CuI↓+I2 |
|
NA表示阿伏加德罗常数,下列说法中正确的是 | |
| [ ] | |
A. |
3.6g D2O中所含质子数为2 NA |
B. |
1 mol FeBr2与足量的Cl2反应转移2 NA个电子 |
C. |
1 mol NH3分子中共价键总数为3 NA |
D. |
4.48 L N2和O2的混合气体所含分子数为0.2 NA |
|
13 C-NMR(核磁共振)、15N-NMR可用于测定蛋白质、核酸等生物大分子的空间结构.下面有关13C、15N叙述正确的是 | |
| [ ] | |
A. |
13 C与15N有相同的中子数 |
B. |
13 C与C60互为同素异形体 |
C. |
15 N与14N互为同位素 |
D. |
15 N的核外电子数与中子数相同 |
|
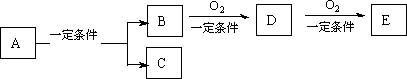
如下图,B为常见金属或非金属单质,有下列转化关系:
若C是可用作自来水消毒的气体,D、E是氧化物,D转化为E时,增加氧的质量约是D物质总质量的25.8%,则A是 | |
| [ ] | |
A. |
NaCl |
B. |
AlCl3 |
C. |
H2O2 |
D. |
KCl |
|
在一密闭容器中发生如下反应:aX(g)+bY(g) | |
| [ ] | |
A. |
升高温度,正反应速率增大,逆反应速率减小,平衡向正反应方向移动 |
B. |
若通入稀有气体使容器体积增大,平衡不移动,则a+b=c |
C. |
若容器中气体的密度不再改变,则反应一定达到平衡 |
D. |
保持容器的体积不变,增加X的量,平衡向正反应方向移动,X的转化率增大 |
|
高铁酸钾是一种高效绿色水处理剂,其工业制备的反应原理是Fe(OH)3+ClO-+OH-=FeO42-+Cl-+H2O(未配平).下列叙述正确的是 | |
| [ ] | |
A. |
ClO-是还原剂 |
B. |
1 mol Fe(OH)3得到3 mol电子 |
C. |
反应配平后,H2O的化学计量数为4 |
D. |
用高铁酸钾处理水时,用到了其强氧化性,且其还原产物能水解生成具有强吸附能力的胶体 |