|
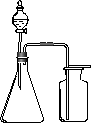
利用下列各组中的物质制备并收集少量相应的气体,能采用如图装置的是
①浓氨水和固体NaOH制NH3 ②大理石和浓盐酸制CO2 ③过氧化氢溶液和二氧化锰制O2 ④稀硝酸和铜片制NO ⑤浓盐酸和二氧化锰制Cl2 ⑥电石与水制C2H2 ⑦锌粒和稀硫酸制H2 ⑧乙醇和浓硫酸制C2H4 | |
| [ ] | |
A. |
②③ |
B. |
①⑥⑦ |
C. |
②⑤⑧ |
D. |
①④⑥ |
|
以下各物质间的每步转化不能通过一步反应就实现的是 | |
| [ ] | |
A. |
C→CO→CO2→Na2CO3 |
B. |
Fe→Fe3O4→Fe(OH)3→FeCl3 |
C. |
Na→Na2O2→Na2CO3→NaOH |
D. |
N2→NO→NO2→HNO3 |
|
1919年,科学家第一次实现了人类多年的幻想——人工转变元素.这个核反应如下:
下列叙述正确的是 | |
| [ ] | |
A. |
|
B. |
|
C. |
O2和O3互为同位素 |
D. |
通常情况下,He等稀有气体化学性质都很稳定 |
|
原子序数依次相差1,且由小到大排列的A、B、C、D、E五种短周期元素.下列是有关这五种元素的叙述: ①若A的最高价氧化物的水化物是强碱,则E的最高价氧化物的水化物是强酸 ②若A的单质既能与强酸又能与强碱反应且都放出氢气,则这五种元素在同一周期 ③若A的阳离子比E的阴离子少8个电子,则D一定是非金属元素 ④若D的最高价氧化物的水化物是强酸,则E的单质在常温下为气态 ⑤若B的单质是原子晶体,则B的氧化物是分子晶体 其中正确的是 | |
| [ ] | |
A. |
①②③ |
B. |
②③④ |
C. |
③④⑤ |
D. |
②④⑤ |
|
下列有关叙述正确的是 | |
| [ ] | |
A. |
1 L 0.1 mol·L-1的醋酸中有6.02×1022个CH3COO- |
B. |
1 mol葡萄糖分子中含有3.01×1024个-OH |
C. |
电解1 L饱和食盐水,当pH=10时,反应中有6.02×1022个电子转移 |
D. |
一定条件下将2 mol SO2和1 mol O2混合充分反应,有2.408×1024个电子转移 |
|
已知c(H+)=1×10-3 mol·L-1的一元酸HX溶液和c(OH-)=1×10-3 mol·L-1的一元碱YOH溶液混合后溶液呈中性,下列判断正确的是 | |
| [ ] | |
A. |
若HX是弱酸,YOH是强碱,则两溶液浓度相等 |
B. |
若HX是强酸,YOH是弱碱,则两溶液体积相等 |
C. |
若HX是弱酸,YOH是强碱,则两溶液体积一定是V(HX)>V(YOH) |
D. |
在混合后的中性溶液中,c(X-)=c(Y+) |
|
莫尔盐[(NH4)2Fe(SO4)2·6H2O]常作氧化还原滴定法的基准物质,在1 L 0.1 mol·L-1的该盐溶液中,下列有关比较正确的是 | |
| [ ] | |
A. |
c(H+)=c(OH-)+c(NH3·H2O) |
B. |
c( |
C. |
c( |
D. |
c( |
|
由下列事实分别得出的结论正确的是 | |
| [ ] | |
A. |
氯气与铁反应生成氯化铁,说明氯气的氧化性强 |
B. |
苯酚与少量碳酸钠溶液反应生成碳酸氢钠,说明苯酚的酸性比碳酸强 |
C. |
甲、乙两种金属用导线连接插入稀硫酸中,电流计指示甲为负极,说明乙是不活泼金属 |
D. |
饱和Na2CO3溶液中通入过量CO2,析出NaHCO3固体,说明NaHCO3的溶解度小于Na2HCO3 |
|
下列叙述不正确的是 | |
| [ ] | |
A. |
往下水道中倾倒硫酸铜溶液,会进一步加快铁制管道的腐蚀 |
B. |
在空气中,钢铁的表面涂一层油脂或油漆,可以减慢钢铁的腐蚀 |
C. |
镁与稀盐酸反应剧烈,加入醋酸钠晶体可以减慢反应速率 |
D. |
铜放入稀硫酸中,再加入硝酸钠可以加快铜与稀硫酸的反应速率 |