|
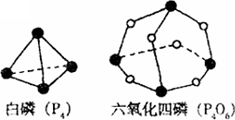
化学反应可视为旧键断裂和新键形成的过程.化学键的键能是形成(或拆开)1mol化学键时释放(或吸收)的能量.已知白磷(P4)和P4O6的分子结构如下图所示;现提供以下化学键的键能:P—P198KJ·mol-1、P—O360kJ·mol-1、氧气分子内氧原子间的键能为498kJ·mol-1则P4+3O2===P4O6的反应热△H为
| |
| [ ] | |
A. |
+1638kJ·mol-1 |
B. |
-1638kJ·mol-1 |
C. |
-126kJ·mol-1 |
D. |
+126kJ·mol-1 |
|
已知Ba(AlO2)2可溶于水.右图表示的是向Al2(SO4)3溶液中逐滴加入Ba(OH)2溶液时,生成沉淀的物质的量y与加入Ba(OH)2的物质的量x的关系.下列有关叙述正确的是
| |
| [ ] | |
A. |
a~b时沉淀的物质的量:Al(OH)3比BaSO4多 |
B. |
c~d时溶液中离子的物质的量:AlO2-比Ba2+多 |
C. |
a~d时沉淀的物质的量:BaSO4可能小于Al(OH)3 |
D. |
d~e时溶液中离子的物质的量:Ba2+不可能等于OH- |
|
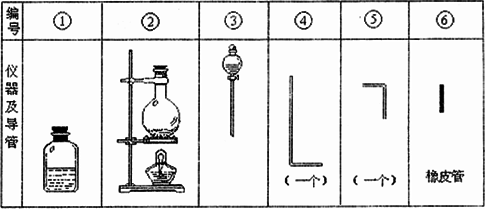
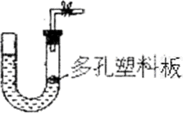
将氯气用导管通入较浓的NaOH和H2O2的混和液中,在导管口与混和液的接触处有闪烁的红光出现.这是因为通气后混和液中产生的ClO-被H2O2yc还原,发生激烈反应,产生能量较高的氧分子,它立即转变为普通氧分子,将多余的能量以红光放出. 进行此实验,所用的仪器及导管如图,以下各回答不正确的是
| |
| [ ] | |
A. |
组装氯气发生器时,应选用的仪器及导管是③②⑤(数字为表中仪器及导管编号) |
B. |
实验进行中,按气流方向从左到右的顺序,气体流红的各仪器及导管的编号依次是②④⑥⑤① |
C. |
仪器①的橡皮塞上应有2个孔. |
D. |
实验时仪器①中ClO-与H2O2反应的离子方程式是:ClO-+H2O2=Cl-+O2↑+H2O |
|
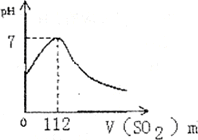
在标准状况下,向100mL氢硫酸溶液中通入二氧化硫气体,溶液pH变化如图所示,则原氢硫酸溶液的物质的量浓度为
| |
| [ ] | |
A. |
0.5mol/L |
B. |
0.05mol/L |
C. |
1mol/L |
D. |
0.1mol/L |
|
将相同质量的铜分别和过量浓硝酸、稀硝酸反应,下列叙述正确的是 | |
| [ ] | |
A. |
反应速率:两者相同 |
B. |
消耗硝酸的物质的量:前者多,后者少 |
C. |
反应生成气体的颜色:前者浅,后者深 |
D. |
反应中转移的电子总数:前者多,后者少 |
|
某非金属单质A和氧气发生化合反应生成B.B为气体,其体积是反应掉氧气体积的两倍(同温同压).以下对B分子组成的推测一定正确的是 | |
| [ ] | |
A. |
有1个氧原子 |
B. |
有2个氧原子 |
C. |
有1个A原子 |
D. |
有2个A原子 |